中国移动强势进入医疗器械领域
2021-07-14
据天眼查APP显示,日前中国移动通信集团有限公司获得了“便携式彩色超声仪器”外观设计专利,公告号CN306650066S,申请日期为2020年10月。据专利摘要说明,本外观设计产品作为便携式彩色超声仪器使用,用于医疗检测。

01
5G远程超声系统助力疫情防治
早在2020年疫情爆发初期,中国移动就利用自身的通讯优势,与深圳华大智造合作,在武汉雷神山医院部署了5G远程超声系统,供隔离区的患者展开肺部的检查。
利用5G远程超声系统,坐镇在北京解放军总医院的专家就可以通过操作机械臂,对雷神山医院的隔离患者展开检查。既及时的采集了患者的信息,又避免了接触感染。据医生反馈,实时回传的画面精准流畅,细节清楚。此外中国移动还向全国多家抗疫医院提供了5G远程会诊系统,医疗服务机器人、疫情防控系统等服务。
02
远程医疗弥补资源缺口
而这也不是中国移动在远程医疗的第一次尝试。2019年3月16日,跨越3000公里,历经3个小时,位于解放军总医院海南医院的神经外科主任医师凌至培为中国人民解放军总医院的一位患者完成了“脑起搏器”植入手术。这是中国移动携手中国人民解放军总医院,完成的全国首例基于5G的远程人体手术。
5G在医疗行业的应用不止于此,在移动政企医疗分论坛中,华大集团国内区域规划与发展中心副主任、华大基因科技创新中心CEO刘靓指出:目前基层医疗机构在医疗资源上存在诸多痛点,例如“硬”件设施不足,“软”件人才缺乏等问题。以超声为例,整体注册医师12万余人,缺口至少还有15万。华大智造和中国移动还将继续合作,推动远程超声影像、基因检测等远程医疗解决方案,促进优质医疗资源的进一步下沉,推动大数据人工智能在生命健康领域的应用。
03
中国移动积极布局移动医疗市场
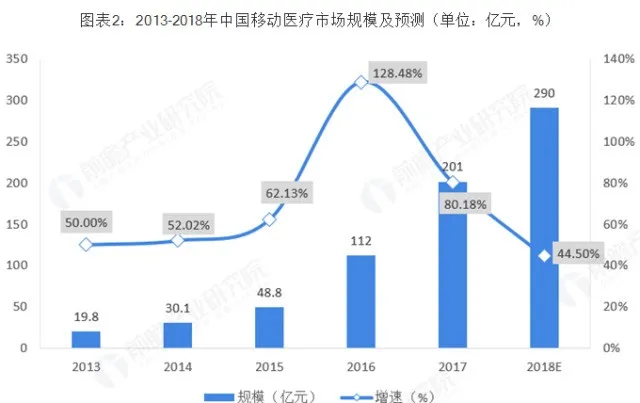 资料来源前瞻产业研究院
资料来源前瞻产业研究院
近年来移动医疗市场快速增长,市场规模从2013年的19.8亿元增长至2018年的290亿元,移动运营商预计会在未来占据移动医疗的主要市场。
中国移动也早早布局,2019年4月,经过两年筹备由国家卫生健康委员会部署、中国移动牵头组建了联仁健康医疗大数据科技股份有限公司,总投资20亿,中国移动持股49.5%,成为第一大股东,中国太平洋人寿保险股份有限公司、济南国际医学中心发展有限公司分列第二第三大股东。
联仁健康业务主要覆盖“健康医疗大数据”、“互联网医疗健康”、“健康医疗产业园”三大板块。这家公司以大数据技术创新为核心,向民众、医院、企业、政府提供健康医疗平台等互联网业务。搭建了先进的“1湖3台”数据架构,通过建设统一标准的数据湖,搭建数据中台、技术中台、开放平台,支撑不同领域的数据应用,建立运营保障体系、安全体系,为丰富应用夯实平台与技术基础。在官网上可以看到,公司还获得了多项计算机软件著作权登记证书。
联仁健康正与医疗行业各机构、产业合作伙伴开展广泛合作,共同建设健康医疗大数据生态圈,推动形成健康医疗服务新模式、新业态,全力以赴助力建设“健康中国”。目前这家公司已经在山东和北京成立了两家分支机构,预计规模还会继续扩大,也相信数字化创新会给整个医药行业的发展提供动力。
来源:医械世界











