从数据获取到机器学习-智能注塑的新机会!
2022-03-21
随着IIoT(Industrial Internet of Things,工业物联网)技术的飞速发展以及成本的迅速下探,注塑行业的数据收集以及监控系统已经比较成熟,各大独立厂商(比如RJG)、辅机厂商、热流道厂商和注塑机厂商等都开发了各种传感器以及数据收集系统,获取注塑生产中的各种数据来指导生产。
但是,这些数据被收集起来之后怎么用成为困难各大厂商及用户的大问题,随着人工智能领域的不断发展,人们似乎是找到了将工业物联网数据效用最大化的出路。
概念流程
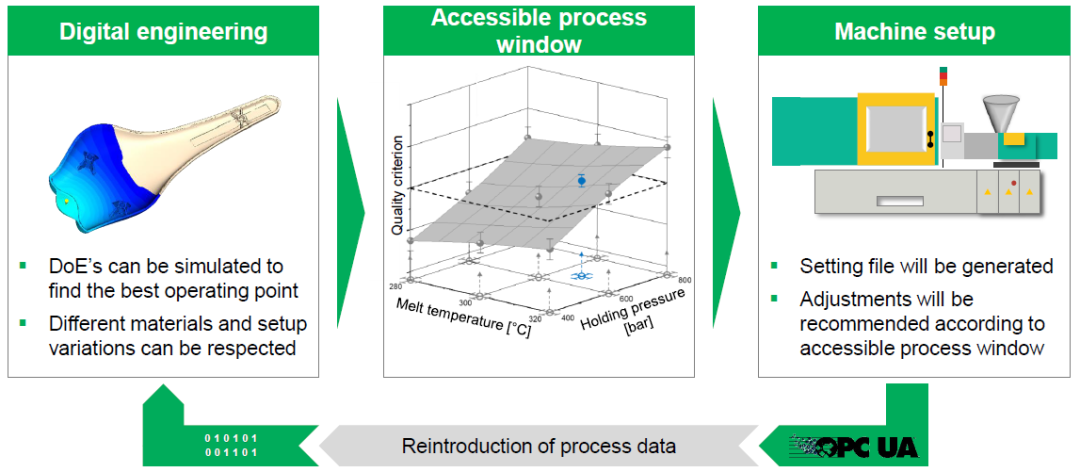
在整个概念流程中,首先,在数字工程部分,模型可根据DoE算法模拟出对应塑胶产品的最佳工艺点。然后生产对应的可操作的工艺窗口,工艺窗口随之生成对应的注塑机设定参数。根据注塑机的实际输出(产品的尺寸,外观等)再反馈到数字工程部分,以进一步优化DoE的结果。
在整个循环过程中,实际的机台参数、数据结果和仿真结果都需要对标,从而提高预测的精度。
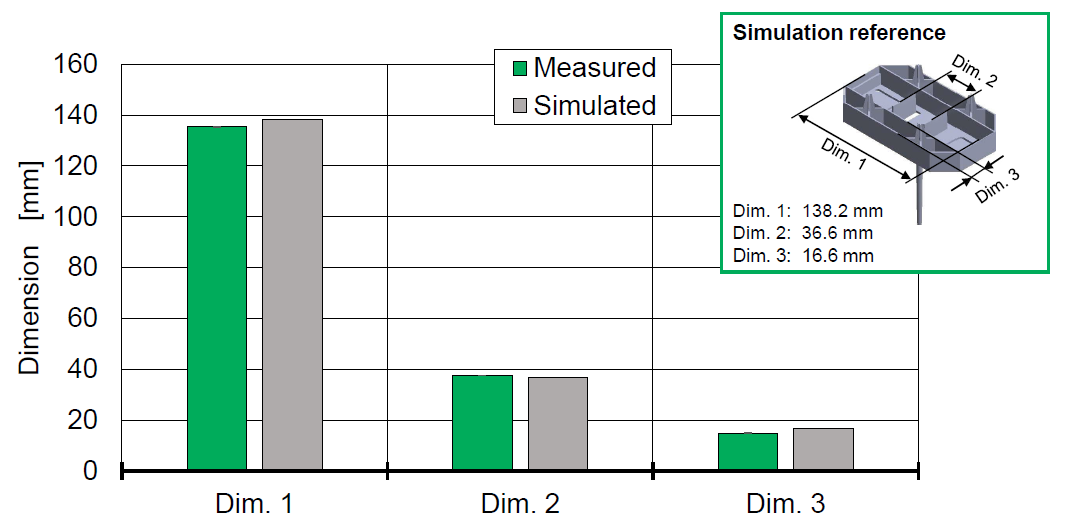
如上图所示,绿色部分为实际产品的三个关键尺寸的测量结果,而灰色部分为前期仿真的尺寸。通过对各个尺寸的虚实对标,可以通过机器学习的算法优化整个模型的精度。
神经网络与参数设定
神经网络是一种模仿动物神经网络行为特征,进行分布式并行信息处理的算法数学模型。这种网络依靠系统的复杂程度,通过调整内部大量节点之间相互连接的关系,从而达到处理信息的目的。
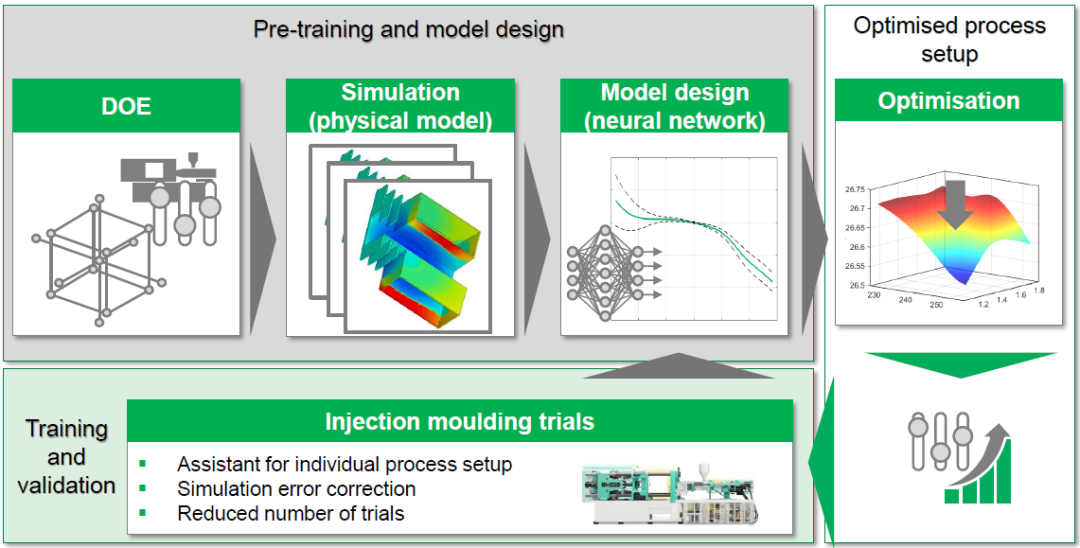
在注塑领域,可以使用预先训练过的模型来,计算出最优的工艺设定参数。如上图所示,预先训练的模型包括DoE、模流仿真和神经网络模型。然后系统将模型计算出的结果生成具体的注塑机工艺设定参数(速度、压力、温度、时间等等)。通过数据传输通道将参数输入注塑机控制系统,注塑机生成产品,然后对产品进行尺寸、外观及性能的测试,并将测试的结果反馈到神经网络模型,进行算法优化和迭代。
这样操作的优势包括:
能够协助具体产品工艺的开发;
模流仿真结果优化;
大幅降低试模次数,真正让T0量产成为可能。
具体案例
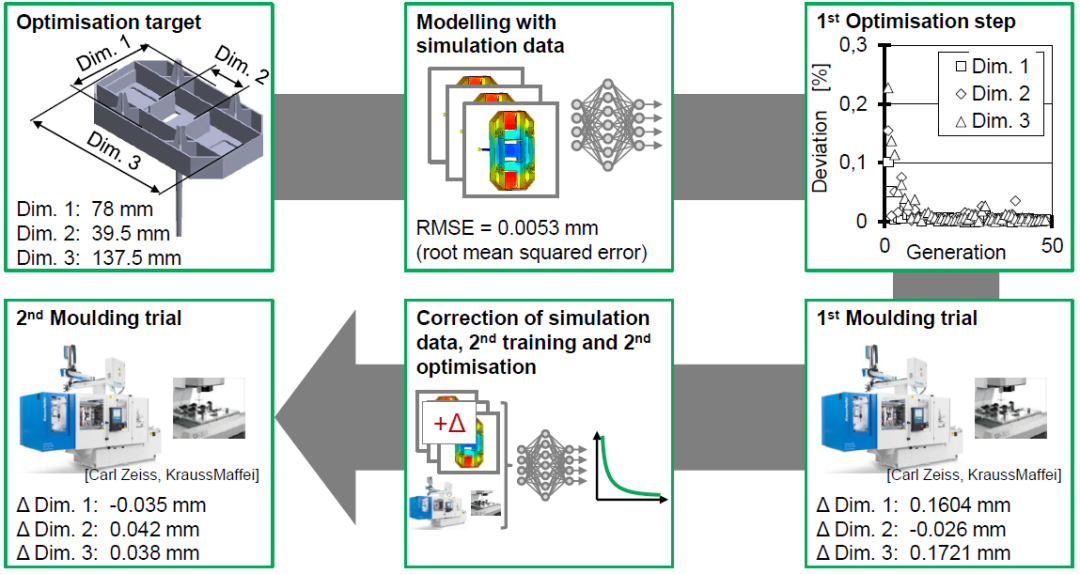
上图案例完整地展示了从3D模型确定、模流结果计算、第一次生成参数、第一次试模、模流数据优化,模型二次训练以及二次生成参数,第二次试模的全过程。相对于第一次试模,三个关键尺寸(Dim.1, Dim.2, Dim.3)的一致性得到大幅提升。
结论
人工智能改变制造业的趋势无法逆转,发展速度近两年会迎来高潮。
在注塑领域,机器学习算法需要解决“小”数据的问题,即如何通过预先训练的算法基于较小的数据样本训练出可用的算法。
注塑机不开放输入接口,算法再好也没用。未来可能会出现两种发展方向,头部较大的几家注塑机厂商大概率会自研(或者收购)成熟的算法公式以提高自有品牌注塑机的性能。而其它没有能够自研或者收购的厂商可能会和第三方算法公司合作。
来源:大注塑











