2024医疗器械展会提醒:又一项新指导原则发布,助力哪些医疗器械细分领域崛起?
2024-04-15
在之前发布的《重磅!又一项新注册审查指导原则发布,创新医疗器械审评高质量发展再提速》和《速览|浅析医疗器械可用性工程的合规性》两篇文章中,我们介绍了可用性工程的基本概念、中外医疗器械可用性工程政策,并重点梳理了国家药监局器审中心3月19日发布的《医疗器械可用性工程注册审查指导原则》及其使用说明的内容要点。同时中国医疗器械市场发展速度迅速,国家愈发重视医疗器械行业的发展,并采取《“十四五”医药工业发展规划》《“十四五”医疗装备产业发展规划》等强有力措施推动行业发展,医疗器械市场整体呈现增长态势。其经过多年的发展,已经形成了一个规模庞大、结构合理、技术先进的产业体系。
这些重磅政策的发布及市场的不断成熟,对医疗器械研发的各个环节及细分市场将产生深远影响,本文继续对医疗器械可用性工程及最新指导原则进行深入分析与解读,并剖析其对行业的影响。
医疗器械的可用性工程是一种关注如何设计和优化医疗器械,以确保其在医疗环境中易于正确、安全、有效地使用的工程学领域,贯穿医疗器械研发、使用、管理的全生命周期,对医疗器械的可用性工程分析如下:
(1)设计阶段
-
用户参与:在设计过程中引入医疗专业人员和最终用户的反馈,确保医疗器械符合他们的需求和操作习惯。
-
人机界面:设计简洁直观的人机界面,包括按键、显示屏和指示灯等,以降低误操作风险。
-
可操作性:考虑医护人员的工作流程和操作习惯,设计器械使其易于操作和快速上手。
-
错误预防:通过设计防错机制、警示系统和容错设计,降低误用风险,提高安全性。
(2)使用阶段
-
培训与教育:提供全面的培训和教育,确保医护人员熟悉器械的正确使用方法。
-
反馈机制:建立反馈机制,收集医护人员和患者对器械使用过程中的问题和建议,以便进行改进。
-
维护与保养:设计易于维护和保养的医疗器械,确保其长期稳定运行。
-
监测与评估:定期监测和评估医疗器械的性能和可用性,及时发现问题并进行改进。
(3)管理阶段
-
风险管理:建立风险管理体系,对医疗器械的使用过程进行风险评估和控制,确保安全性。
-
质量控制:建立质量控制体系,确保医疗器械符合相关标准和规定,提高可靠性。
-
改进流程:持续改进医疗器械的设计和使用流程,以提高效率和安全性。
医疗器械的可用性工程需要综合考虑设计、使用和管理等多个方面,以确保医疗器械在医疗实践中发挥最大效益,提高医疗质量和安全性。
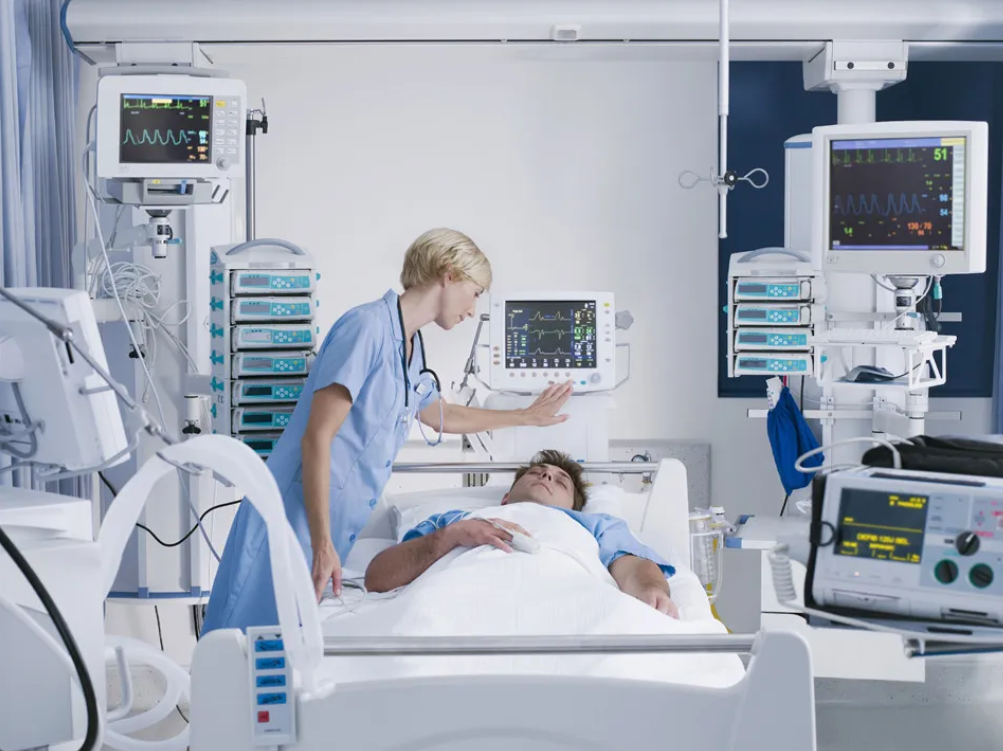
医疗器械可用性工程审评指导原则的解读
-
用户中心设计:强调将最终用户的需求和体验置于设计的核心位置,确保医疗器械的设计符合用户的操作习惯和认知方式,提高用户满意度。
-
风险评估:在设计过程中全面评估潜在的风险和安全问题,采取相应的措施降低误用和意外事件的发生概率,确保医疗器械的安全性。
-
人机工程学原则:遵循人机工程学原则,设计简洁直观的人机界面,考虑用户的认知负荷和操作便捷性,降低使用错误的可能性。
-
培训和支持:设计易于理解和操作的医疗器械,同时提供相关培训和支持,确保医护人员熟练掌握正确的使用方法,降低误操作的风险。
-
反馈和改进:建立反馈机制,收集用户的意见和建议,持续改进医疗器械的设计和功能,以适应不断变化的用户需求和医疗环境。 -
标准合规:确保医疗器械符合相关的标准和法规要求,包括人机工程学标准、医疗器械安全标准等,保障医疗器械的质量和安全性
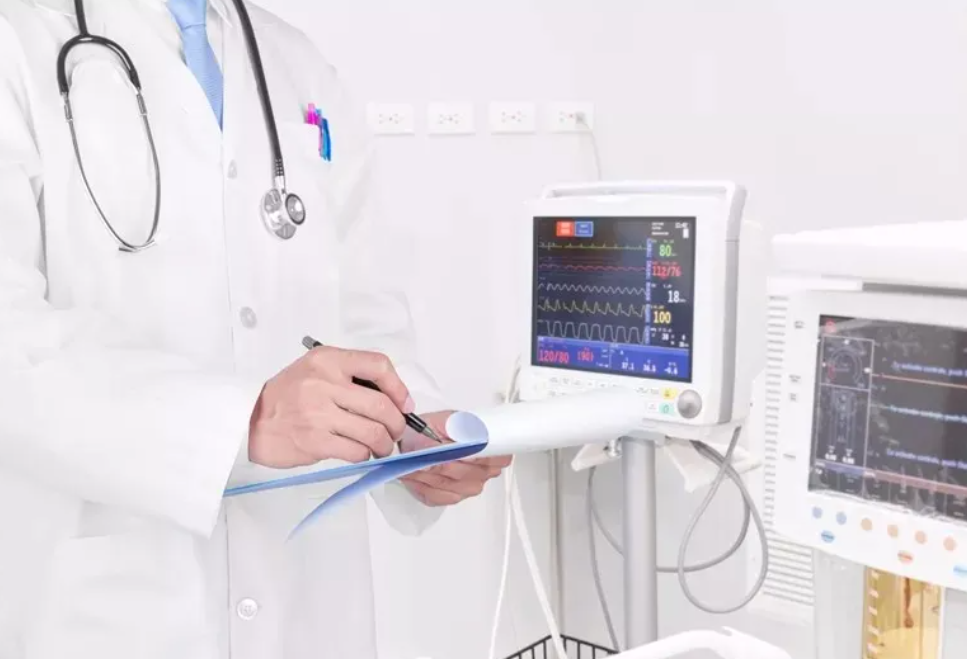

其次,对于中低风险医疗器械领域,虽然要求相对较低,但也需要根据产品指导原则的要求提交相应的注册申报资料,这包括使用错误评估报告等,旨在评估产品在使用过程中可能出现的错误和潜在风险,从而采取相应措施进行改进。这有助于提升中低风险医疗器械的可靠性和安全性,降低用户在使用过程中可能遇到的风险。
(3)对整个医疗器械行业发展的影响
技术创新和研发投入:医疗器械可用性工程审评指导原则的实施需要企业加大对技术创新和研发投入。为了提高产品的可用性,企业可能需要不断进行技术改进和更新,以满足市场对更先进、更实用的医疗器械产品的需求。
例如,开发更加智能的呼吸机,能够根据患者的呼吸状况自动调节参数,实现个性化的治疗。这种技术创新有助于推动呼吸机市场的进步和发展。
行业规范和标准提升:可用性工程审评指导原则的推广和实施有助于推动整个医疗器械行业规范化和标准提升。行业内企业都遵循相同的可用性工程审评标准,可以有效降低产品的设计和生产风险,提高产品质量,共同促进行业的良性发展。
此外,医疗器械可用性工程审评指导原则还促进了人因设计在医疗器械领域的应用和发展。人因设计强调综合运用关于人类的解剖、生理、心理、行为等方面能力与限制的人因知识来设计开发医疗器械,以提升产品的可用性和用户体验。随着该指导原则的推广和实施,越来越多的医疗器械制造商开始关注人因设计,将用户的需求和体验纳入产品设计和开发过程中,从而推动医疗器械产品的创新和升级。
总而言之,医疗器械可用性工程审评指导原则对细分领域市场的影响将在提高产品设计水平、增强市场竞争力、推动技术创新和规范化标准等方面展现出积极的作用。
文章来源:











