全球“首个”全人工心脏 | 上海医疗器械博览会展望这一产业新布局
2023-12-27
近日,上海医疗器械博览会Medtec China 2024了解到世界最先进的全人工心脏设计者和开发商CARMAT,宣布开设其位于Bois-d’Arcy的第二个生产基地(BDA2)正式投入使用,目前该基地工厂已完成,所有的设施安装均已通过公告机构DEKRA的审查,该建筑及其设施符合医疗器械的最高生产标准,此外,该项目的投产将使公司从 2024 年起达到每年 500 个 Aeson® 全人工心脏的生产能力。人工心脏又称心脏辅助装置,以前作为在等待心脏移植供体过程中的过渡治疗,经过几代的发展,目前其已经具有很高的质量和疗效,已经成为又一治疗心衰的“终极”方法。
这座 1,500 m 2 的新生产基地,将使 CARMAT 能够在以下方面显著提高其产能:Aeson® 心脏电子部件的组装,产品和制造过程的微生物测试,接收和检查传入的组件,储存和运输。
结合“BDA1”工厂目前正在完成的洁净室扩建工程,“BDA2”工厂的启用将使公司能够按计划在2024年初达到500颗心脏的年产能。
CARMAT 首席执行官 Stéphane Piat评论道:“我们新生产设施的启用是一项重大成就,凭借历史悠久的“BDA1”设施和新的“BDA2”设施,我们拥有了高性能制造工具,经认证,从 2024 年起每年可生产多达 500 颗心脏。根据我们的战略计划,我们将进一步在未来几年内发展我们的工业设施,到 2027 年达到年产 1,000 颗 Aeson® 心脏的产能。”
法国Carmat成立于 2008 年,由现代瓣膜手术之父的Alain Carpentier、Matra Défense(空中客车集团)Truffle Capital风投公司联合创立。
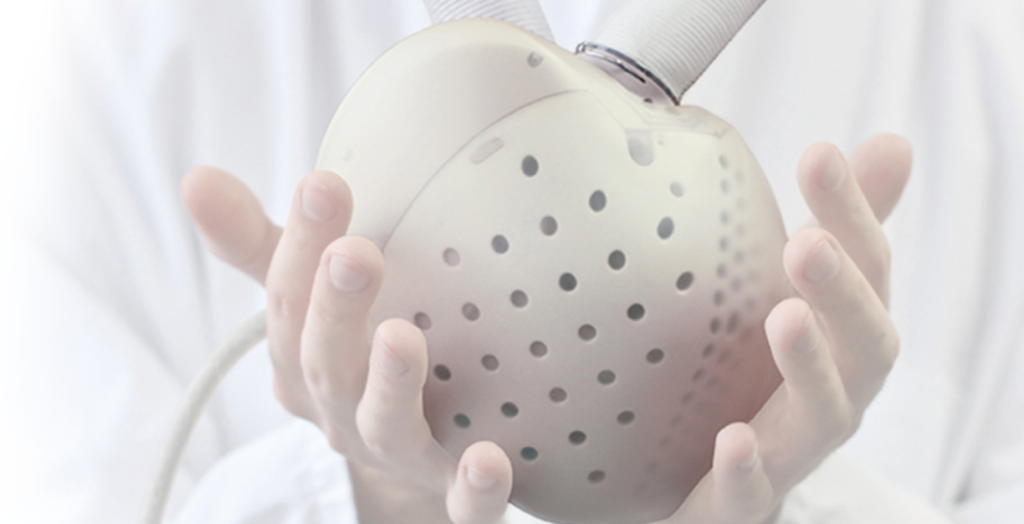
Carmat开发的Aeson人工心脏是一种有源植入式装置,旨在替代晚期心力衰竭患者的原生心脏心室,其形状与人类心脏的形状相对应,由两个腔室组成,使用牛心包膜将血液隔室与液压流体隔室分开,植入装置的患者可能不需要抗凝治疗,是全球第一个高度血液相容性、脉动性和自我调节的生物合成人工心脏。一旦Aeson ® Heart连接起来,它就会复制原生心脏的动作,提供机械循环支持并恢复身体的正常血液流动。
Aeson ®目前仅在欧洲上市,它被认为是终末期双心室心力衰竭(Intermacs 1-4 级)患者进行移植的桥梁,这些患者均是无法通过的药物治疗或左心室辅助装置 (LVAD) 中来治疗。植入后需要 180 天内进行心脏移植,在美国,Aeson ®目前只能通过临床试验获得。
在2013年,Carmat 获得法国国家药品与健康产品安全局的授权后,于同年12月18日在欧洲成功进行了全球首次人工心脏植入手术。2017年,Carmat在欧洲交易创业板alternext市场上市,股票发行价为18.75欧元。2020年2月,Carmat 公司在获得FDA的批准后,开始在美国对 10 名符合移植条件的患者展开临床可行性研究。2020年12月,Carmat 的人造心脏获得欧洲CE认证,并以 Aeson 的名义在欧盟和其他认可CE 标志的国家销售。
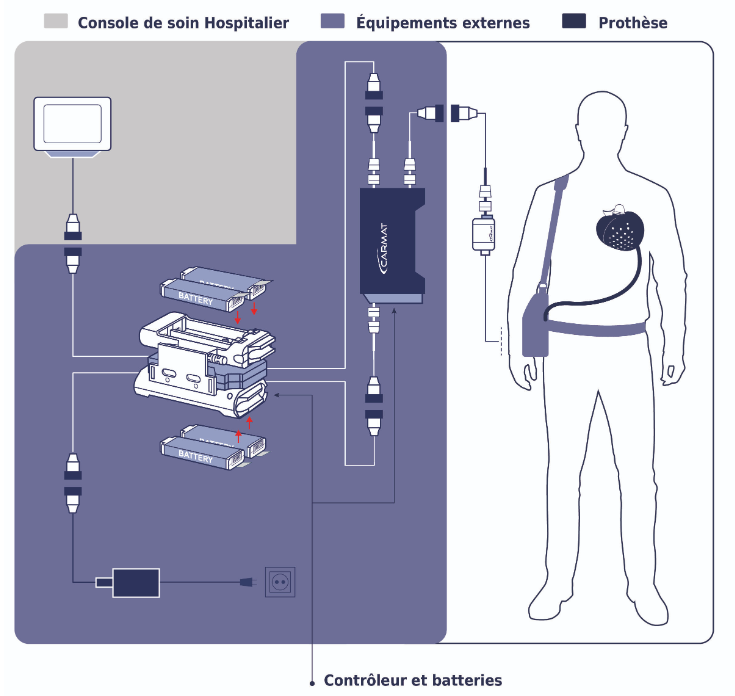
人工心脏作为人工制成的一种精密仪器,有着医械“皇冠上的明珠”称号。通过在解剖学、生理学上使心脏产生有节律地收缩,不断泵出血液以供应人体的需要,从而实现替代人体因重症丧失功能不可修复的自然心脏的一种人工脏器。根据市场种类划分为心室辅助装置 (VAD)和全人工心脏(TAH)两大类型。
当前全球布局全人工心脏的仅有寥寥几家,同时所有全人工心脏均未在国内获批上市。全人工心脏目前主要是两家公司,一家是美国的Syncardia公司,另一家就是Carmat公司。SynCardia 全人工心脏于2004 年获 FDA 批准使用,法国Carmat 的全生物人造心脏于2020年获得欧洲CE认证。此外也有创新独角兽企业BiVacor正不断崛起。
植入介入属于高端医疗器械下面细分品类,从《中国制造2025》到《健康中国2030规划纲要》,高端医疗器械国产化已经达到了前所未有的国家战略高度。为更好助力企业的创新突破,上海医疗器械博览会Medtec China 2024同期举办ADTE高端有源医疗装备技术展,近120+企业已加入展区助力产品制造智能、高效。点击立刻参展。
SynCardia Systems成立于2001年,目前隶属于Picard Medical,其开发的 TAH-t(曾用名CardioWest、Jarvik-7)主要用于终末期双心室衰竭的情况下临时替换原生心脏和四个瓣膜,已被植入约2 000例患者。目前,SynCardia正在通过SPAC完成上市。

图 SYNCARDIA 临时全人工心脏(TAH-T)
SynCardia 全人工心脏于2004 年获 FDA 批准使用,Syncardia研发的人工心脏是世界上唯一获FDA批准上市的全人工心脏,由双心室及四个瓣膜结构构成。作为用作晚期心力衰竭患者心脏移植前的过度治疗手段,在临床上已应用已经有着35年的历史。该公司目前共有两款人工心脏、两款体外驱动器,从而为不同类型的患者提供医疗支持。目前,Syncardia TAH在全球植入数量达到2049。
BTAH全人工心脏是首个基于旋转血泵技术的植入式全人工心脏,可用于长期治疗严重双心室心力衰竭患者(并非真正代替人类心脏)。
美国BiVacor成立于2008年,总部位于休斯敦,该公司开发了一种连续流全人工心脏,由一个单独的磁悬浮叶轮组成,位于分开的左右心室之间,该装置的特点是圆盘的轴向位置可以根据负载条件而改变,从而实现类似生理上 FrankStarling(心力衰竭中的代偿机制)的反应。BiVacor TAH旨在接管患者衰竭心脏的全部功能,是一种长期设备,可以取代患者天然心脏的全部功能。
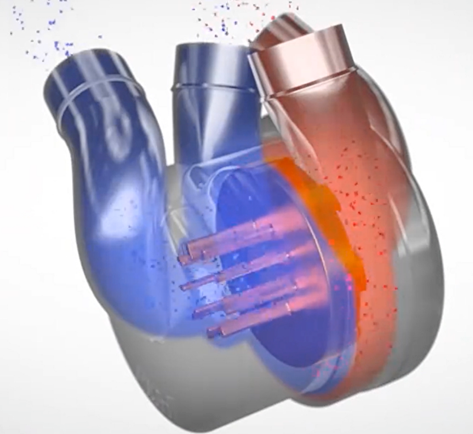
图 BiVacor人工心脏
2023年3月,iVACOR宣布完成一轮1800万美元融资,用于支持其临床前人工心脏设备的持续开发以及BiVACOR TAH早期可行性临床研究。本轮融资由Cormorant Asset Management和OneVentures领投。同时BiVACOR宣布预计在今年年底进行其核心产品BiVACOR TAH首次临床可行性研究。
11月30日, BiVACOR宣布FDA批准其产品—BiVACOR TAH进行IDE研究。据悉 与其他全人工心脏相比,BiVACOR TAH通过3D打印技术制造,其材料为钛,钛已经在临床上被验证过材料,具有优异的生物相容性。而特殊设计的泵体大间隙可有效减少血细胞损伤,降低血栓的风险。BiVACOR TAH由于采用“磁悬浮”技术,避免内部零件的摩擦或机械磨损,使其具有更长使用寿命,至少有10年。(目前已上市的人工心脏,更多是作为心脏移植前的过渡技术,而非真正替代心脏)
TAH 是一种植入在患有双心室心力衰竭或左右心室功能障碍患者体内的医疗器械,这种病例占心力衰竭患者的 5% ~30%,其余为左心衰竭。根据目前已上市的TAH价格均在100万人民币左右,假设市场渗透率只有1%,市场规模也会超过百亿,属于真正意义上的蓝海市场。
上海医疗器械博览会Medtec China 2024了解到目前国内日趋火热的人工心脏更多是左心室辅助装置(LVAD),其只能治疗左心衰。当患者同时患有左心衰和右心衰时,心室辅助装置就无法治疗该患者。对于国内的患者来说无法及时进行心脏移植就能等死,这种情况下全人工心脏的作用就显得意义非凡。但高难度的技术、较难展开的临床试验使得全人工心脏TAH的发展始终保持低速度。尽管TAH已经投入商用,技术上也在逐渐进步,但全球的总体移植数还是很少。首要原因就在于高昂的价格。人工心脏加上手术、术后排异药物的费用,这是一笔不小的开支。其次是心脏移植的不可逆性。安装TAH之前会摘除掉患者原有的大部分心脏,这个过程是不可逆的,许多患者在心理上还是不敢用一颗机械心。
心衰不是一种独立的心脏疾病而是各种心脏疾病发展到严重阶段的一种临床综合症,由于心脏功能衰退,心脏排血量减少不能满足身体各组织器官需要。其病情严重易反复、终末期生存率低,持续增长的患者数量让心衰疾病成为21世纪心血管疾病的最大挑战。对于终末期心力衰竭患者而言,心脏移植是最佳的治疗手段,但人体心脏供不应求。
截止至2020年,中国的心衰患者人数达到了890万人,60岁以上人群心衰患病率超过3%,心衰患者平均每年住院30天,人均年住院费用29746元。心衰由于具有难治疗、预后差的特点,已经成为不可忽视的健康问题,也成为巨大的公共卫生负担。
对于未来,下一代TAH应具有良好的持久性、提高生存获益和更低的不良事件发生率,以期其可以作为长期支持使用发展到作为目的治疗使用。此外,高昂的造价费用也使得众多患者望而却步,产品的持久性及进一步降低价格,也成为未来全人工心脏需要攻克的市场门槛。
文章来源:医疗器械创新网
参考:和义广业创新平台、医林研究院、中投同和











