2022年苏州医疗器械展会医疗器械监管新规解读之一 ——医疗器械GCP修订亮点
2022-09-26
一、引言
近年来,我国医疗器械行业不断迭代发展并向国产替代的目标跃进。2021年2月9日,国务院发布了修订后的《医疗器械监督管理条例》(“《条例》”),随着《条例》、优化医疗器械审批审评等法律文件和多项改革政策的相继出台,作为《条例》配套管理规范之一—2016年6月1日实施的《医疗器械临床试验质量管理规范》(“《医疗器械GCP(2016年版)》”)也需进行相应的修订。对此,国家药监局和国家卫健委于2022年3月31日联合发布了最新修订的《医疗器械临床试验质量管理规范》(“《医疗器械GCP》”)。
2022年苏州医疗器械展会速递本文,将于近期针对医疗器械监管体系中的配套新规进行专题性解读,本文将围绕《医疗器械GCP》核心修订亮点展开,主要包括对强调临床试验各参与方的职责与临床试验质量控制、明确多中心临床试验开展各项规定、优化安全性信息报告流程及其他事项报告备案要求及明确将体外诊断(“IVD”)试剂纳入《医疗器械GCP》管理等修订亮点进行深入解读,并对《医疗器械GCP》出台后的行业影响予以对应分析总结。
同时在现场2022年苏州医疗器械展会Medtec China 将围绕法规建设、医疗器械创新审批、上市前和上市后监管等策划会议,从行业、监管和企业角度解读中国医疗器械法规及企业的应对。
二、《医疗器械GCP》核心修订亮点解读
相较于《医疗器械GCP(2016年版)》,《医疗器械GCP》框架从11章96条调整为9章66条,其中,临床试验前准备、受试者权益保障、试验用医疗器械管理、基本文件管理等章节内容统一划归到了临床试验各参与方职责章节中。《医疗器械GCP》更强调临床试验各参与方的职责与对临床试验的质量控制,按照总则、临床试验各主体职责、临床试验方案与实验报告、多中心临床试验、记录要求的次序来安排章节内容,框架结构更加科学、合理、有序。
本文以下对《医疗器械GCP》核心修订亮点内容进行对应解读。
(一)强调临床试验各参与方的职责与临床试验质量控制
1.强调临床试验各参与方职责
医疗器械临床试验参与方涉及的主体包括伦理委员会、临床试验机构、研究者、申办者、受试者、合同研究组织(“CRO”)等。考虑到CRO为申办者或临床试验机构的受托方或服务方,《医疗器械GCP》中主要对伦理委员会、临床试验机构、研究者【1】与申办者的主体职责与义务及对于受试者权益的保障进行规制。实践中,医疗器械临床试验各参与方法律关系或基础职责具体如下图所示。
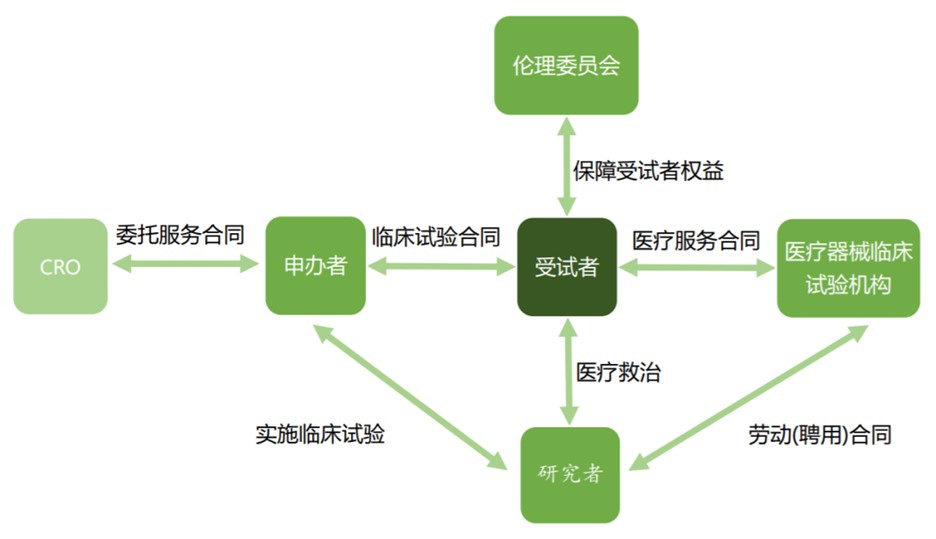
《医疗器械GCP》更加强调临床试验各参与方的职责与义务及对临床试验的质量控制,规范试验过程。具体而言:
1.1.完善伦理委员会职责与要求
《医疗器械GCP》将“伦理委员会”相关内容从《医疗器械GCP(2016年版)》中的第五章前移至总则之后的第二章,位于各参与方主体之首,与《药物临床试验质量管理规范》(“《药物GCP》”)体例保持一致,同时也对伦理委员会的相关规定进行了修订,吸收了原国家卫生计生委于2016年发布的《涉及人的生物医学伦理研究审查办法》中对伦理委员会职责的表述,对于医疗器械临床试验受试者权益保障愈发充分,具体表现为:
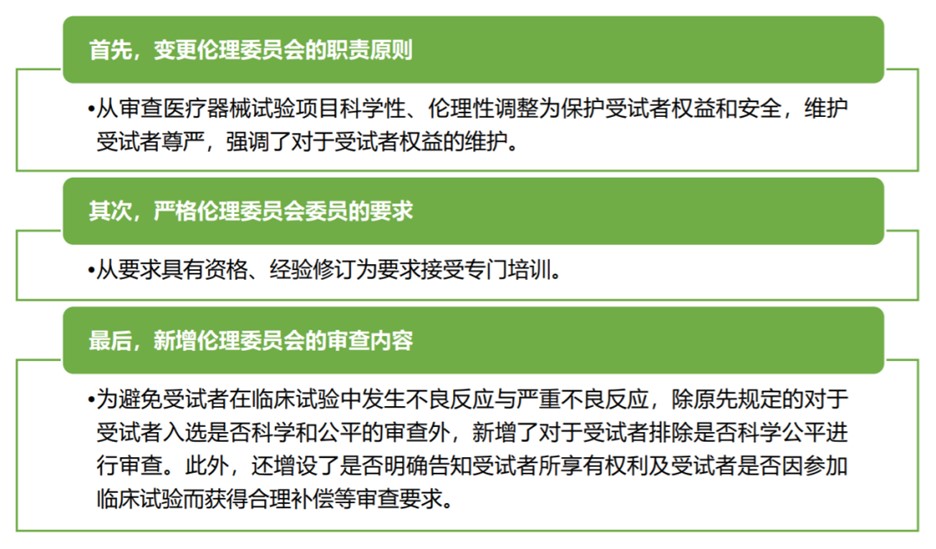
1.2.突出申办者主体责任
根据《条例》规定,医疗器械注册人、备案人应对研制、生产、经营、使用全过程中医疗器械的安全性、有效性依法承担责任【2】。对此,《医疗器械GCP》对申办者提出了更高的要求,突出申办者主体责任,引入了风险管理理念,要求申办者建立覆盖医疗器械临床试验全过程的质量管理体系,确保医疗器械临床试验符合相关法律法规,保护受试者权益和安全,前述修订实质上是医疗器械注册人制度在临床试验阶段的落实。
具体而言,《医疗器械GCP》进一步强调了申办者对医疗器械的管理职责,包括在规定的条件下将试验医疗器械运输至医疗器械临床试验机构,对从医疗器械临床试验机构回收的试验医疗器械负责保存回收处置等记录。此外,《医疗器械GCP》第42条、43条还明确了申办者为受试者免费提供试验医疗器械、支付临床试验相关费用及发生损害或死亡时的补偿职责等。
更多医疗器械法规以及监管条例解读,请关注2022年苏州医疗器械展会Medtec China同期法规峰会:中国医疗器械法规更新与应对,议题覆盖新修订的《医疗器械监督管理条例》及相关配套新政览读、医疗器械质量管理信息化、有源医疗器械临床评价常见问题、医疗器械突发事件应急处置与媒体沟通演练。点击点击快速预登记。
1.3.优化医疗器械临床试验机构职责与要求
《医疗器械GCP》优化了医疗器械临床试验机构的基本资质条件和要求,包括删除了《医疗器械GCP(2016年版)》中“医疗器械临床试验应在两个或两个以上医疗器械临床试验机构中进行”的要求,同时规定医疗器械临床试验机构资质只需满足“具备相应条件且按照规定备案”,无需再进行资质认定,解决了实践中部分医疗器械难以且无需在两家临床试验机构开展临床试验的问题,简化了机构资质审查要求,为临床试验开展提供了便利。
此外,《医疗器械GCP》对医疗器械临床试验机构职责提出了更为严格的要求,包括明确临床试验机构的职责定位,要求医疗器械临床试验机构应建立临床试验管理组织架构和管理制度,具有相应的临床试验管理部门,承担医疗器械临床试验的管理工作【3】。具体而言,《医疗器械GCP》第19条至第21条明确了临床试验机构具有机构备案信息系统填报、临床试验前评估、伦理委员会审查前组织评估主要研究者资质并完成备案、建立涵盖临床试验实施的全过程质量管理制度、保存临床试验记录和基本文件等职责义务。
1.4.明确研究者职责与要求
基于行业实践需求,《医疗器械GCP》首次区分了主要研究者与研究者。其中,《医疗器械GCP》第24条明确要求了主要研究者应具备相应的资质条件,并完成备案;第27条对参与试验的研究者增加了应具有临床试验经验与参加申办者组织的与该临床试验相关的培训等要求。此外,《医疗器械GCP》第30条、33条、34条还新增了研究者对生物样本管理的职责及主要研究者处理安全性信息与向伦理委员会报告临床试验的进展的职责。
2.对临床试验管理更精细严格
在医疗器械注册环节,医疗器械临床试验数据的真实准确对于医疗器械安全有效性的判定及是否满足上市条件极为重要,因此,医疗器械临床试验数据的真实性和合规性一直以来都是医疗器械临床试验的监管重点之一。自2016年起,原国家食药监总局曾多次组织开展医疗器械临床试验监督抽查,对在审的医疗器械注册申请中的临床试验数据的真实性、合规性开展监督检查,查处临床试验违法违规尤其是弄虚作假行为,并对相关抽查结果进行公告【4】。例如,国家药监局于2020年11月,对在审的10个医疗器械注册申请项目开展临床试验监督抽查,涉及27家临床试验机构。其中,杭州某生物科技公司生产的某联合检测试剂盒被发现在浙江大学医学院附属第一医院开展临床试验中,医疗机构留档的电子照片拍摄时间、地点与临床试验实际时间、地点不一致,临床试验数据无法溯源。对此,国家药监局对该医疗器械不予注册,并自不予注册之日起一年内不予再次受理该项目的注册申请的处理结果,同时责成浙江省药监局依法依规进行相应调查处理【5】。
由此可见,国家愈发重视对于临床试验数据的监管并严厉打击医疗器械临床试验弄虚作假行为。对此,《医疗器械GCP》也细化了对于生物样本、试验数据记录、文件管理在内的临床试验各环节的管理,相关监管内容也更为精细严格。
此外,《医疗器械GCP》还明确第III类医疗器械临床试验要求,并将临床试验各环节的“核查”严格为“稽查”等,强化了监管措施,也为监管部门开展医疗器械临床试验合规检查及企业进行自查提供了明确的指导,具体如下简表所示:

(二)明确医疗器械多中心临床试验开展各项规定
近年来,我国吸引愈来愈多的全球生物制药公司在中国开展国际多中心临床试验,我国的国际多中心临床试验数量由2015年的46项(占全球国际多中心临床试验总数的10.4%及中国所进行临床试验总数的13.6%)大幅增至2019年的156项(占全球国际多中心临床试验总数的19.7%及中国所进行临床试验总数的15.1%)【6】。随着国内外研究合作愈发频繁与国家间开展医疗器械多中心临床试验的情形日益增多,我国对多中心临床试验的监管需要进一步明确和细化。
《医疗器械GCP》的出台充分体现了这一趋势与国家对医疗器械研发创新的重视,将多中心临床试验通过专门章节进行规制。同时,相关管理规则与国际接轨,借鉴国际医疗器械监管者论坛(IMDRF)的监管协调文件相关内容,如吸收IMDRF MDCE WG/N57 FINAL:2019《临床试验》内容,引入在不同国家或地区开展的多区域临床试验的概念,在《医疗器械GCP》正文和术语多处体现了国际标准最新版本内容,有利于全球创新产品同步在中国开展医疗器械临床试验【7】。具体而言,《医疗器械GCP》对于多中心临床试验相关规定进行了如下增改:
首先,明确了多中心临床试验的定义。多中心临床试验中按照同一临床试验方案实施临床试验的医疗器械临床试验机构的数量从原先的“三个以上(含三个)”变更为“两个以上(含两个)”【8】,也即,目前在两个医疗器械临床试验机构实施的临床试验也属于多中心临床试验。
其次,引入了多领域临床试验的概念。多中心临床试验在不同的国家或地区实施时,为多区域临床试验【9】。值得注意的是,在中国境内实施多区域医疗器械临床试验应符合我国《医疗器械GCP》的相关要求,进一步强调了我国《医疗器械GCP》在监管制度层面的重要性。 再次,细化了多中心临床试验的要求。具体包括:确保各中心均能遵守临床试验方案;强调各中心临床试验方案的一致性;强调各中心使用相同病例报告表记录试验数据;以书面明确各中心职责;确保各中心主要研究者之间的沟通;确定临床试验协调研究者与组长单位,承担各中心的协调工作【10】。
最后,调整了多中心临床试验报告及分中心临床试验小结签章要求。报告的签署者由研究者变更为协调研究者,报告的审核、交付者由临床试验管理部门变更为组长单位医疗器械临床试验机构,分中心小结签署者由研究者变更为主要研究者,分中心小结交付对象由牵头单位变更为申办者【11】等。
(三)优化安全性信息报告流程及其他事项报告备案要求
1.优化安全性信息报告流程与要求
医疗器械临床试验过程的安全性是《医疗器械GCP》的重点监管内容,本次修订优化了安全性信息报告相关流程,突出和强调申办者主体责任,同时对于安全性信息根据严重程度进行了更为科学细致的划分,并据此提出了更为明确的报告时限。
首先,在安全性信息报告流程方面,将原先的申办者和临床试验机构“双报告”调整为申办者“单报告”。根据《医疗器械GCP》,在获知试验医疗器械相关严重不良事件(“SAE”)等安全性风险信息后,应由申办者向所在地省级药监部门及医疗器械临床试验机构所在地省级药监和卫生健康部门报告,并采取风险控制措施。
其次,在安全性信息报告时限方面,将SAE区分为(1)死亡或危及生命的SAE及(2)非死亡或非危及生命的SAE和(3)其他严重安全性风险信息,并针对不同安全性事件调整并明确报告时限【12】。安全性信息报告相关规定修订内容具体对比总结如下:
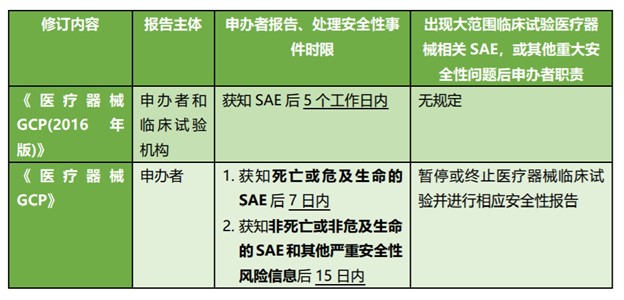
2.优化其他事项报告备案要求
此外,《医疗器械GCP》还优化了其他事项报告备案相关要求,例如,取消了原检验报告1年有效期的要求,明确了临床试验项目备案时间要求,明确临床试验终止或完成后报告时限等,整体更有利于临床试验的顺利开展。
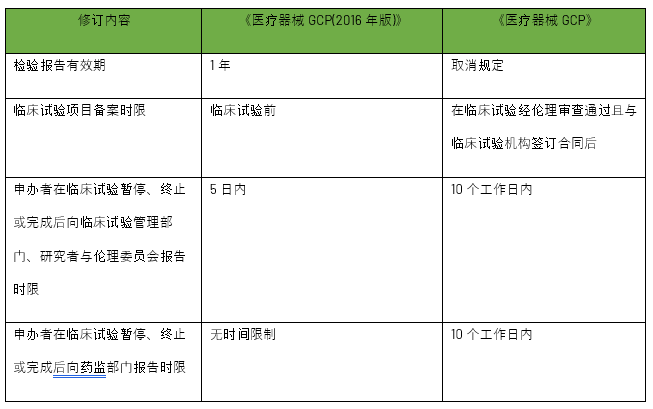
(四)其他修订亮点
除上述核心修订亮点外,《医疗器械GCP》还将IVD试剂纳入统一管理,同时强调临床试验全流程对受试者的权益保护。
1.IVD试剂纳入《医疗器械GCP》管理
根据统计数据,我国2019年IVD试剂市场规模已增长至864亿元,占医疗器械市场规模13.9%,预计至2022年,我国IVD市场规模将达到1,460亿元,占医疗器械市场规模比例将达到15.9%【13】。面对IVD巨大的市场需求与行业的飞速发展,IVD临床试验也亟需更为精细化的管理规范。国家药监局于2021年9月16日发布的《体外诊断试剂临床试验技术指导原则》中,便有IVD试剂临床试验应符合医疗器械GMP相关要求的规定。
对此,《医疗器械GCP》扩大适用范围,将IVD试剂临床试验质量管理要求正式纳入统一管理规范,包括:(1)为申请IVD试剂注册而实施的临床试验相关活动,应遵守本规范【14】;(2)对于医疗器械临床试验机构,也明确规定包含了承担IVD试剂临床试验的血液中心和中心血站、设区的市级以上疾病预防控制机构、戒毒中心等非医疗机构【15】。此外,也需注意,《体外诊断试剂临床试验技术指导原则》中对于IVD临床试验设计、试验机构、试验报告撰写、质量管理细节等方面的要求进行了细化补充,在实践中同样应作为IVD设计和开展临床试验的依据之一。
但值得注意的是,在注册与备案环节,于2021年8月26日出台的《医疗器械注册与备案管理办法》与《体外诊断注册与备案管理办法》两个文件将IVD试剂与其他医疗器械进行了区分,适用不同的管理办法加以规制。
2.强调临床试验全流程对受试者的权益保护
受试者是临床试验开展全流程的核心主体。上述提及《医疗器械GCP》强调临床试验各参与方的职责与加强临床试验质量控制等规定,为临床试验过程中受试者权益保障的落实和体现,此外,《医疗器械GCP》还强调在医疗器械临床试验备案完成后,该医疗器械临床试验机构方可开始第一例受试者知情同意及筛选【16】,体现了临床试验开展前对受试者权益的保护。
三、《医疗器械GCP》出台后总结和展望
《医疗器械GCP》将于2022年5月1日正式施行,为医疗器械临床试验确立了新的合规标准,对加强临床试验管理、受试者权益保护起到了重要积极作用,也为医疗器械临床试验的规范发展和质量提升提供指引和依据,将进一步促进医疗器械行业创新和高质发展。
一方面,《医疗器械GCP》简化优化了包括安全性信息报告、检验报告等在内的部分流程与要求,更有利于临床试验的开展。另一方面,此次修订也进一步加强了对医疗器械临床试验的监管,强调临床试验各参与方的要求职责与临床试验质量控制,为受试者权益与试验安全提供了更为充分的法律保障。其中,医疗器械研发企业应关注申办者的主体责任,明确自身职责与义务,同时重点关注临床试验数据记录的可追溯性要求,确保临床试验过程科学规范、结果真实可靠,减少未来撤销医疗器械注册或备案证明等法律风险。
与此同时,《医疗器械GCP》明确了多中心临床试验开展的各项规定,为我国将来开展多中心临床试验奠定了制度基础,同时积极转化适用国际医疗器械监管协调文件,与国际监管制度接轨,细化了多中心临床试验的开展要求,使我国医疗器械临床试验管理体系更加规范、科学和完善。此外,《医疗器械GCP》的出台让IVD临床试验监管也将有据可参,体现了国家重视与鼓励IVD行业创新发展的趋势,同时也对IVD临床试验监管提出了更加细致严格的要求。临床试验机构、研究者及伦理委员会应关注上述规定的变化调整,了解自身在临床试验全流程的职责及加强临床试验各阶段行为的合法和规范性,保障受试者安全和权益,以减少违规风险。
当然,临床试验仅作为医疗器械研发环节的重要组成部分,根据医疗器械生命周期,本团队下篇文章将围绕《医疗器械注册与备案管理办法》的修订亮点内容展开,对医疗器械注册与备案环节的监管规则进行相应分析解读,欢迎各位读者持续关注。
来源: 威科先行











