首款无创血糖仪获医械注册,产品深度技术解析
2019-12-26
“ 2019年8月26日,博邦芳舟医疗科技(北京)有限公司与清华大学历经十年合作开发的“无创血糖仪”获由国家药品监督管理局颁发的首张“无创血糖仪”医疗器械注册证(属国家第三类医疗器械,注册证编号:国械注准20193070602)。”

血糖仪经过了半个多世纪的发展,历经了数次改进,从干化学方法到电化学方法,但目前侵入性的有创血糖仪仍然占领了整个血糖检测市场。由于惧怕疼痛,以及由此引发的心理恐惧,有创的测量方式直接导致极大一部分糖尿病患者放弃固定的血糖检测。因此,有创血糖仪问世后不久就有学者提出了无创血糖仪的概念,几乎同时就开展了无创血糖仪的研究工作。
无创血糖仪由此也成为了众多科学家心中“皇冠上的明珠”。可以预见,如果无创血糖仪技术成熟,将对目前的自我血糖监测(SMBG)甚至动态血糖监测CGMS市场格局产生巨大的影响。
下面我们以博邦芳舟的产品为例对无创血糖仪做一些分析。

博邦芳舟采用的是代谢热整合法,即通过与人体代谢相关的参数来得到血糖浓度。该原理最早由两位美国学者(Seaman,G.V.F.;Engel, R.;Swank, R.L.Hissen)于1965年在《自然》杂志中发表的文章中提出。
O.K.CHO(US.Pat.NO.5975305和US.Pat.NO.20060094941等)公开了一种基于代谢率热整合法的热-光学无创血糖检测方法。该方法假设体内的热量来源于代谢释放的能量,而代谢的主要能源物质是糖类,绝大多数组织细胞通过葡萄糖的有氧氧化过程产生和获得能量。由于在平衡状态下,(静态)产热量和散热量在数值上相等,那么通过测量血氧总量和散热量等生理参数就可以估计血糖值。如下图所示,将各个传感器的信号输入CPU,通过特定的算法得到血糖浓度。
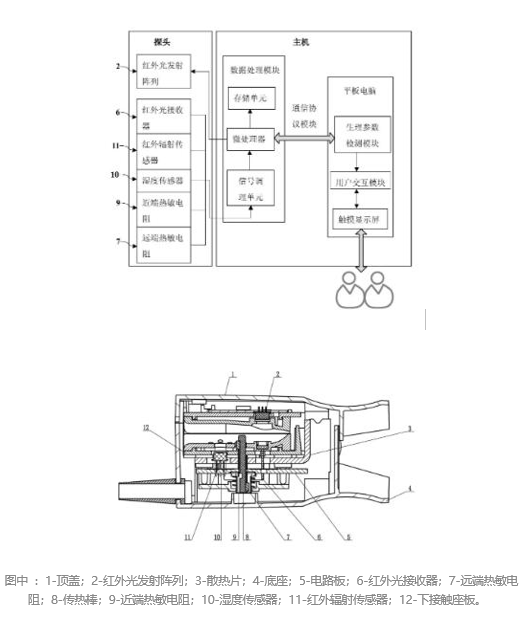
图中 :1-顶盖;2-红外光发射阵列;3-散热片;4-底座;5-电路板;6-红外光接收器;7-远端热敏电阻;8-传热棒;9-近端热敏电阻;10-湿度传感器;11-红外辐射传感器;12-下接触座板。
检测探头处于自由状态(即不与人体被测部位接触)时,红外辐射传感器6和湿度传感器10分别测量的是环境辐射温度T2和环境湿度D2,而将检测探头夹持于人体被测部位(如手指、 耳朵等)时,红外辐射传感器6和湿度传感器10分别测量的是人体被测部位辐射温度信号T1和周围湿度信号D1,与此同时,导热棒15与被测部位(如手指、耳朵等)相接触,随即发生热传递现象,由于温度发生变化,近端热敏电阻7与远端热敏电阻8的阻值会发生变化,该变化后的阻值信号R1和R2被温度检测电路所检测;发光二极管13发射的光波通过被测部位(如手指、 耳朵等)后产生透射光谱信号A1~A4,由光波接收器14接收, 弹簧所产生的压力信号P由压力传感器12测得。
然后,这些测量元件测得的量分为三路传输到数据处理与显示系统:人体被测部位辐射温度信号T1、环境辐射温度信号T2、被测部位周围湿度信号D1、环境湿度信号D2和压力信号P通过传输线依次经过放大滤波电路和A/D转换电路进入微处理器;
近端热敏电阻7和远端热敏电阻8的阻值信号R1、R2通过传输线进入温度检测电路,电阻信号转变为温度信号,然后温度信号经放大滤波电路和A/D转换电路进入微处理器;
透射光强信号A1~A4依次经过一阶放大滤波电路、积分电路以及二阶放大滤波电路进入微处理器。发光二极管13的工作由发射器控制电路来控制,该发射器控制电路通过控制线路与微处理器相连接;一阶放大滤波电路由电位器开关电路来控制,该电位器开关电路通过控制线路与微处理器相连接;二阶放大滤波电路则直接通过控制线路与微处理器相连接。这样,发射器控制电路、一阶放大滤波电路以及二阶放大滤波电路都受到微处理器的控制。
在微处理器的参与和控制之下,所有信号都传输到微处理器中,这些信号按照本发明的无创血糖检测原理进行数据处理,从而得到仪器所测量的血糖值大小。血糖值以及关键的中间数据通过传输线路分别输入到显示单元和存储单元,实现数据的显示和存储功能。微处理器作为数据处理的核心单元,有如下三个作用:一是采集所有数据,并进行运算处理;二是产生控制信号, 对发射器控制电路、二阶放大滤波电路和电位器开关电路进行控制;三是将数据输送到显示单元和存储单元,分别完成显示和存储。
上述技术分析基于博邦芳舟专利,和实际产品可能会有不同。
来源:器械之家











