医疗设备展带你一文读懂微波消融技术与器械
2022-06-29
微波技术几十年前就被用于军事、通讯领域,以后又被用于勘探、医疗等领域,近年来更在肿瘤消融治疗领域大放异彩。目前,微波消融(microwave ablation,MWA)作为成熟的治疗技术,已被广泛用于微创手术中,并因其微创、安全、手术时间短、恢复快等优点,受到越来越多的临床医生和患者的肯定和认可,许多观众医疗设备展Medtec China,首先,微波是一种低能量电磁波,波长范围0.001-0.3米,频率范围为约900至2,450MHz(也有写为1,000-300,000MHz,但实验室和家用一般2,450MHz)。参考下图2,微波能量带有在正负值间振荡的电荷,可产生快速交变电场,而生物组织内的水分子(H2O)自带电荷。当水分子暴露于微波源的振荡电荷时,作为小电偶极子的分子会在空间来回翻转,努力与相反极性的电磁电荷对齐。因此,微波可通过以下两种模式与分子相互作用:偶极旋转和离子传导。在偶极旋转中,分子不断来回旋转,每个旋转分子间的摩擦产生热量。而在离子传导中,自由离子或离子物质在空间中平移,试图与交变电场对齐,与偶极旋转一样,这些运动物质间的摩擦也能产热。
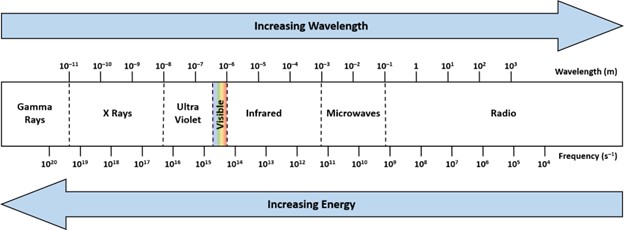
图1 电磁频谱
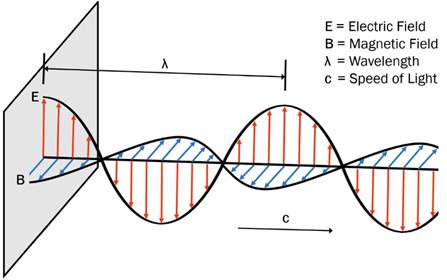
图2 微波的组成成分
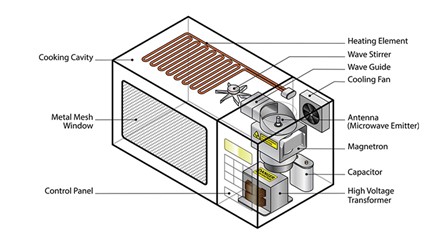
图3 家庭用微波炉的常见设计
尽管都通过热介导的凝固性坏死来破坏组织,但MWA与射频消融RFA并不同,主要为其能量沉积机制不同,如下图3。RF消融为电流通过离子组织介质时,通过电阻加热产生热量,因此RF消融加热需要导电途径,仅限于低导电性区域,且只会引起电极邻近的组织加热。而MWA能够有效传播并加热许多类型的组织,即便其为低电导率、高阻抗或低热导率(这也是MWA无论相比RF、电穿孔还是冷冻消融的优势所在,它能够穿透脂肪),例如骨骼与肺,等等。
和所有能想到的消融方式一样,20余年前即有MWA运用于心肌组织的报道,含水量相对较高的心肌组织具有高导电性,MWA相比RFA可在更大深度和更大体积上消融组织,且不会出现碳化,因此可能更适合心房颤动和室性心动过速的治疗。从90年代初期开始,工程师和研究者们即在不断地尝试缩小微波天线的尺寸,以适应心内消融。但这一阶段的MWA导管,普遍因过高的导管头端至组织界面的加热,反而限制了体内的功率输送和消融所产生的病变尺寸。(部分研究还显示,在相似设定条件下微波导管与RF导管的比较中,其病变消融深度并不比RF更深,因此随着射频技术的进一步全面发展,MWA的关注度就减弱了)
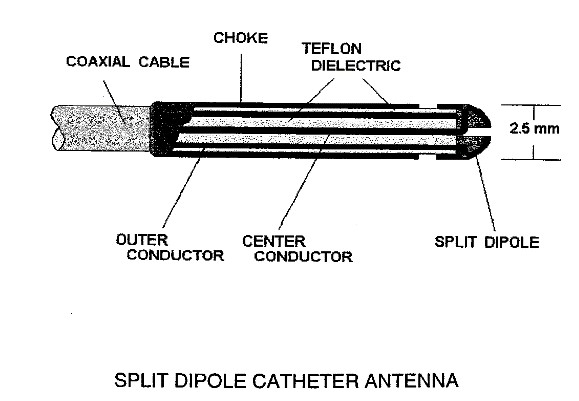
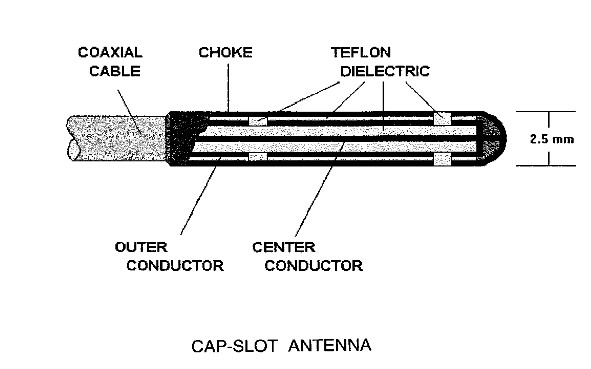
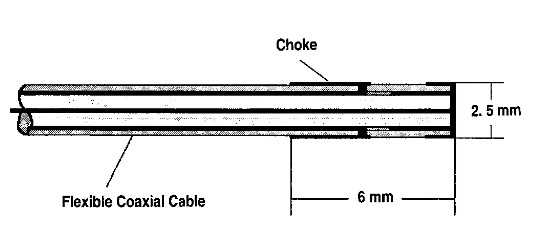
图5 1999年University of Illinois at Chicago的James C. Lin教授报道的,三种微波消融导管的头端设计。由上至下,分体式导管天线设计(Split-tip catheter antenna),帽槽导管天线设计(Cap-slot catheter antenna),和帽锁导管天线设计(Cap-choke catheter antenna)
随后,我们可一步跨到2020年的报道,看看目前的盐水灌注微波消融导管的设计,如下图6来自澳大利亚研究者们的报道。其中,8Fr尺寸可通过Agilis鞘进行心内消融,11Fr则用于心外膜消融,消融期间以30mL/min的速度用盐水灌注。微波功率由可调谐的2.4-2.5GHz GMS2000微波发生器提供,在消融过程中,荧光测量显示头端温度由基线升高<1℃。研究者们将心外膜设定以90-100W消融4分钟,心内膜则以140-180W消融4分钟。最终,体外模型在不伴有心外膜脂肪和肺组织的情况下,90W消融240秒时产生的病灶深度和长度分别为14.8±1.0mm和34.1±2.3mm,480秒时则分别为19.2±0.5mm和36.8±0.1mm。而在动物模型(羊)中的试验显示,16次心内膜消融过程中的3次,和12次心外膜消融中的3次产生了蒸汽爆裂,但没有一个与头端碳化或凝结物有关(提示组织表面温度<80℃)。90-100W 240秒通过心外膜脂肪产生的消融灶平均厚度为1.2mm(IQR,0.8-1.3mm),宽度为18±10mm,长度为29±8mm,距离冠脉的中位距离仅为2.7mm,且每次消融后的冠脉造影均未提示动脉痉挛或闭塞。仅有一只羊出现了肺的消融损伤。心内膜消融的病灶则相对小,平均深度为10.7±3.3mm,宽度为16.5±5mm,长度为20±5mm。
医疗设备展Medtec China已经从2012年开始连续举办了7届植入介入医疗器械峰会,会议围绕骨科植入物、心血管介入产品,探讨其法规政策、市场趋势、研发与设计与材料创新等内容,为医疗器械制造商、材料供应商及服务商等提供国内外的经验借鉴。点击快速预登记,立即获取参会机会。
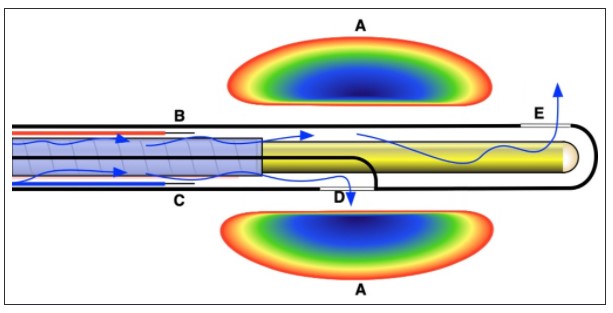
图6 2020年澳大利亚Westmead Hospital的研究者们,设计并完成体外和动物试验的MWA导管头端示意图。A,估算的微波加热场;B和C,两个导线末端连接到单独的充满盐水的腔室,每个腔室在微波天线附近都由自己的出孔,分别为(D)和(E)。在操作过程中,盐水通过蓝色箭头进行灌注,从(C)至(D),以及(B)至(E)的盐水柱形成离子桥,能够在消融部位形成单极或双极感应和起搏,从而无需另加金属线至微波场(由于盐水电极的阻抗较高,起搏输出限制为2mA)
自然,MWA也没有错过大热的肾动脉去神经RDN。在2017年的报道中,仍然是上文这批澳大利亚的研究者(研发个系统不容易,要尽可能多找适应症),尝试开发了介入途径的非接触式微波消融导管,除了消融导管,医疗设备展Medtec China现场还将提供包括高性能医用导管、带封闭式采血系统的血压传感器、血栓抽吸泵系统部分之抽吸导管、TPU一次性切口保护套管、同步扭控弹簧管、薄壁管、FEP易撕热缩管、多色多排管、超声刀内外套管、玛莱克特式导尿管等展品。并认为其能在实现去神经支配的同时,不对肾血管的内膜和中膜造成损伤。其在动物模型中的消融深度为5.9mm,高于EnligHTN和Symplicity同类产品;但在羊肾动脉中消融时,9次有8次出现了导致肾动脉狭窄>50%的肾动脉痉挛。而在对一根曲折肾动脉160W消融后,产生了80%的偏心性狭窄,但随后的组织学检查未观察到透壁性损伤。
来源:MiHeart











