2023年苏州医疗器械展会新“材”必究:微流控制备多组分软性生物材料
2023-01-06
软性生物材料具有良好的可变形性、生物降解性、生物相容性、高生物活性和低抗原性等特点,已被广泛应用于组织工程、再生医学、软体机器人、可穿戴设备和生物诊断等生物医学领域。目前,软性生物材料的发展已呈现出从简单组合到多组分构建的趋势,微流控技术是制备多组分软性生物材料的极佳策略。
2023年苏州医疗器械展会Medtec China了解到中国工程院院刊《Engineering》2022年第6期刊发《微流控制备多组分软性生物材料》一文,总结了基于微流控制备的多组分软性生物材料的最新进展,并介绍它们在生物医学领域的应用;同时,对该领域现存挑战和未来趋势进行了总结与展望。文章首先简要介绍了典型的软性聚合物,主要包括水凝胶和弹性体,以及它们的常见交联方式。接着,描述了如何通过微流控方法将这些聚合物塑造成具有可微调配置的多组分软性生物材料,主要产物形式为多组分颗粒和微纤维。进一步地,详细讨论了这些多组分软性生物材料在生物医学领域的应用。
一、绪论
易于在外部刺激下发生三维形变的软性生物材料(soft biomaterial)在不同领域得到了广泛研究。软性生物材料通常是生物聚合物。它们可以被加工成不同的形状和组成,兼具多种功能特性。与硬质材料不同,软质材料的弹性模量通常低于10 MPa,其特征取决于两个关键因素:结构单元的性质及结构间相互作用。软性生物材料具有独特的性质,如形状记忆、自振荡、可拉伸性以及多种生物相关特性,包括生物相容性、生物降解性、低抗原性和高生物活性。因此,软性生物材料被广泛应用于组织工程、生物医药、体外诊断、电子皮肤和软体机器人等领域。
软性生物材料的发展已呈现出从简单组合到多组分构建的趋势。具有不同成分、尺寸和架构的多组分软性生物材料(multicomponent soft biomaterial)允许集成多样化组件,因此可以适应多种功能。这种复合生物材料可以很好地满足更复杂应用场景的要求。近年来,已经开发出了多种策略以制备多组分软性生物材料。这些方法可以分为“自上而下”和“自下而上”两类。“自下而上”策略是指通过受控自组装、定向生长以及模板合成来构建包括原子、单体和纳米粒子在内的构件。与“自上而下”的方法(即传统的微加工方法,如光刻)相比,“自下而上”的策略在解决固有尺寸限制和加工限制等问题方面具有巨大潜力,并且能以相对较低的成本设计创建任意微结构。然而,传统的大批量合成平台在混合、成核、生长、组装和反应过程中缺乏准确性,难以支持多组分生物材料的批量合成。因此,需要探索出能实现精细化控制的先进制造方法来解决这些限制。
微流控(microfluidic)技术是制备多组分软性生物材料的极佳策略。它将液体限制在几百微米以下的微通道中,并提供亚微升级别的精确流量控制。与宏观系统相比,微流控技术提供了一个受限的微型反应系统,具备均匀的物理化学环境。此外,通过合理设计微流控通道,可以将多相流按照理想方式整合,从而实现产物形态和成分的多样性。这种能力对于制备多组分软性生物材料非常有利,因此,微流控技术已成为可控制备具有复杂微结构和多功能特性的多组分软性生物材料的先进工具。目前应用微流控技术合成出了多种多组分软性微粒、微纤维和复合材料,它们在生物医学领域得到了广泛的应用。
本文概述了多组分软性生物材料的微流控合成及其生物医学应用的最新进展。我们首先介绍了典型的软性生物材料种类及其独特的物理化学性质。接着,我们描述了用于制备多组分软性生物材料的微流控平台构建及其相应产物,聚焦于微粒、微纤维和其他复合材料。我们强调了这些材料的独特成分、形态和显著优点。然后,我们介绍了这些多组分软性生物材料在生物医学领域的应用,包括药物递送、组织工程和生物诊断等,重点突出了微流控合成策略的独特优势。最后,我们深入讨论了微流控技术在制造多组分软性生物材料方面的现存挑战和未来前景。
二、典型软性聚合物
聚合物及衍生复合材料占软性生物材料的大部分,包含天然和人工合成材料。典型的软性聚合物包括水凝胶、弹性体等。水凝胶已成为研究最为广泛的软材料之一。它们的特征是包含亲水性聚合物网络,具有高含水量和良好的生物安全性。同时,水凝胶具有与人体组织接近的杨氏模量,较为柔软。因此,它们在生物医学应用中具有重要价值,如用于药物释放、组织工程和生物诊断。弹性体,尤其是具有相当韧性的弹性体,通常可以在外部刺激下发生变形并恢复其原始形状。水凝胶和弹性体都由移动聚合物链的交联网络构成。几种交联方法已被用于从单体前体制造聚合物材料,没有这些方法,预聚物的机械性能不足,将会对实际应用构成巨大障碍。交联后,相互连接的聚合物链使材料的机械强度及稳定性增强。常见的软性聚合物及其代表性交联方法列于表1。
(一)水凝胶
水凝胶是一种通过物理或化学相互作用交联形成3D网络的亲水聚合物。水凝胶最吸引人的特点之一是它们可以保持水分并维持特定形状,同时能够响应各种外部刺激因素(如pH值、温度、电磁场和生物分子等)而发生变形,并释放水分。水凝胶的湿润特性和刺激响应性与生命组织类似。在对外部刺激作出反应的过程中,水凝胶会发生变化,进而影响和调节其他特性。目前存在种类繁多的水凝胶来源,包括天然产物、合成聚合物、共聚物以及复合混合物等。一些代表性水凝胶的化学结构。
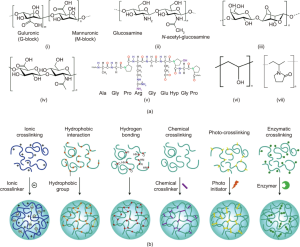
图1. 典型软性聚合物的化学结构及其常见交联方法。(a)藻酸盐(i)、壳聚糖(ii)、琼脂糖(iii)、透明质酸(iv)、明胶(v)、聚乙烯醇(vi)和聚乙烯吡咯烷酮(vii)的化学结构;(b)从单体前体生成软性生物材料的交联方法,包括离子交联、疏水作用、氢键连接、化学交联、光交联和酶交联。
多糖、蛋白质和细菌生物聚合物是可用于构建水凝胶材料的常见天然聚合物。多糖是典型的碳水化合物,由通过糖苷键连接的聚合物组成,根据电荷可以分为阳离子、阴离子和非离子类别。多糖通常具有可电离的侧基,如果胶的羧酸盐、壳聚糖的胺,这决定了它们在某些pH值条件下的电荷密度。多糖的物理化学特性易于通过表面改性进行调整。它们具有良好的水溶性、生物相容性和生物降解性,加之高丰富性和低成本优势,这些特性使它们在多种生物医学场景中具有广阔的应用前景,如有效的药物释放、细胞封装和生物传感器等。
蛋白质通常由通过肽键连接的多个氨基酸残基构成,它们在维持生命活动中起着至关重要的作用,支持并调节着细胞、组织和器官的功能。球状和纤维状蛋白质是其两大类形态。蛋白质的氨基酸序列决定了它的相对分子质量、构象和其他理化特征。蛋白质已被广泛用于制造各种生物医学领域所需的软性生物材料。
除了天然聚合物外,合成聚合物也是水凝胶材料的重要来源。合成聚合物水凝胶的性质不同于天然聚合物,其结构单元具有不同的化学结构。调整合成中涉及的化学成分或参数(即温度、前体浓度、交联方法、交联元素等)会带来全新的性质。聚乙二醇(PEG)是目前应用最广泛的合成水凝胶之一。PEG衍生水凝胶具有良好的生物相容性、溶胀能力和低毒性,是药物递送的优良载体。基于聚乙烯醇(PVA)的水凝胶提供了相对润湿的环境,作为伤口敷料有利于加速创面修复。基于聚乙烯吡咯烷酮(PVP)的水凝胶可以通过简单、清洁的辐射交联获得,也被广泛应用于生物医学领域。以往的研究表明,具有可逆交联和动态网络的水凝胶有着独特的黏弹性,这对于药物输送和细胞调节具有关键意义。这些黏弹性材料可以结合到微流控软性生物材料系统中,例如,将纳米凝胶或纳米复合材料封装到微球或微纤维中将有助于控制这些材料的宏观和微观性质。
(二)弹性体
弹性体是具有类似橡胶弹性的聚合物,它们可以在施加外部载荷时反复变形,并在移除载荷时恢复其原始形状。聚氨酯(PU)、聚烯烃和聚酯是典型的弹性体。它们的弹性主要取决于聚合物的分散性和交联位置的相对分子质量均匀程度。弹性体是智能纺织品、可穿戴设备和软体机器人的关键基材。聚硅氧烷是该领域最常用的聚合物,它具有介电性能优良、易改性、易加工的特点。柔性材料PU拥有高介电常数和出色的耐磨性,而热塑性聚氨酯(TPU)尤其具备突出的形状记忆功能,能够在外部刺激下保持和恢复原形状。
(三)软性聚合物的交联
从单体前体制备聚合物材料的典型交联方法如图1(b)所示。超分子组装体可以由化学物质通过可逆弱分子间相互作用(如离子相互作用、疏水作用力和氢键)结合在一起而形成。例如,在生物聚合物溶液(如藻酸盐和果胶)中添加二价阳离子(如Ca2+),两者通过离子交联快速固化;基于蛋白质(如牛奶蛋白)的热响应水凝胶可以通过疏水相互作用经由热变性制成;对于某些多糖(如琼脂糖),加热后溶液冷却会发生凝胶化,它们通过氢键来稳定3D结构。
化学交联是另一种交联方法,是在反应式官能团之间形成共价键。与通过物理作用结合的凝胶网络相比,通过共价键连接的网络结构相对稳定坚固,通常会在体内环境中表现出更强的机械特性和长时间稳定性。在常规化学交联策略中,席夫碱反应是最广泛使用的方法之一,其核心是在生理条件下在氨基和醛基内产生亚胺键。光交联和酶交联方法因其反应迅速的特点而被应用于原位固化,过程仅需约10 min。
三、微流控制备多组分软微粒
基于微流控技术,不同形式的多组分软微粒被开发出来。微流控平台通过剪切多相流体获得均匀的乳液液滴。微流控技术在微粒制备中具有突出的优势,如对尺寸、形态、表面形貌、成分等的精确控制。目前已经通过乳液液滴模板合成了多种多组分软微粒,包括微球、非球形微粒、中空/多孔微粒、Janus微粒、微胶囊和复杂多核软微粒。
(一)液滴微流控技术
微流控液滴技术最优越的特点是其能够连续生成单分散乳液液滴。液滴的产生可以通过在流体碰撞位置调整两种或多种不混溶的溶液来完成,其中黏性应力和界面张力的存在会导致分散流体夹断,进而得到液滴。调整两相流道的几何形状和流体参数可以很好地控制液滴大小和单分散性。得益于这些优点,液滴微流控已被广泛用于制备包含多组分软性生物材料的微粒。
最广泛采用的微流控通道几何结构是同流式(同轴连接)、流动聚焦式和错流式(T形连接),如图2(a)~(c)所示。在同流式通道中,内相和外相以同心居中方式通过两条管道流动[图2(a)];在流动聚焦式通道中,分散相通过单通道注入并被两股连续相流包围[图2(b)];在T形结构中,两相流体以垂直方向流动[图2(c)]。液滴尺寸可以通过调节分散相和连续相的黏度、流速比、毛细管尖端尺寸和表面活性剂浓度来控制。除了被动法生成液滴之外,研究人员还开发了依赖外力的主动方法,如电磁场、热毛细管、声学等驱动系统。Wang等设计了一种电极驱动的液滴生成装置。首先,液体在电场的驱动下被挤出容器。当电极关闭时,液流形成狭窄颈状并最终被夹断,生成液滴,如图2(d)所示。实际上,微流控中的微液量要求对制造微粒造成了障碍。空气微流体利用射流喷射到空气中产生液滴,并控制射流破裂和聚结,其液滴产生频率是基于芯片的微流控方法的两倍。在这种方法中,如图2(e)所示,液滴列从喷嘴1中挤出,并与从喷嘴2中喷出的射流发生碰撞。
(二)Janus软微粒和多区软微粒
Janus微粒是具有双相几何形状和两个不同组分半球的粒子,该结构赋予单个微粒两组完全不同的物化性质和特征。当两个分散相相互接触并同时被连续相乳化时,可以生成含有两相或多相的液滴。随后通过相分离、聚合、溶剂蒸发等方式固化液滴,制备得到Janus或多区微粒。当两个分散相组分容易相互溶解时,需要对称的通道结构设计确保内相在微流控通道内保持完整的 Janus结构,否则两种成分在形成液滴时往往会发生混溶。当两个内相组分不能相互溶解时,可以忽略两相间的混溶。在这种情况下,除了对称的芯片架构外,不对称几何通道(如T形)也可用于生成Janus液滴,这大大简化了微流控芯片的制造要求。Zhang等通过向多个内相通道注入不同种水凝胶前体溶液,并对生成液滴中的全部溶液进行快速凝胶化,制造出了多区凝胶软微粒。如图3(a)所示,他们首先构建了流动聚焦式PDMS芯片来制造海藻酸盐液滴,当海藻酸盐和外相中的钙(Ca)离子接触时,离子交联固化成不同区室间具有明显界面的软性微凝胶。Maeda等通过集成离心装置和多口毛细管的液滴生成器,展示了一种均匀多区分布的藻酸钙水凝胶微粒的新型制造策略[图3(b)]。他们利用多口毛细管将不同的独立内相流体引导到相同的外相中,将液体剪切成Janus和多区微液滴。
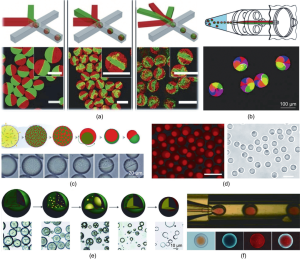
图3. Janus、多区和核壳软微粒的微流控制备。(a)荧光显微图像显示使用微流控芯片制成的多区水凝胶微粒,PDMS芯片具有多个分散相通道(比例尺:100 µm);(b)基于离心驱动和多口毛细管装置生成多区微液滴;(c)橡子状微粒的形成过程;(d)雪人形Janus聚(N-异丙基丙烯酰胺)(PNIPAM)微粒的荧光和光学显微图像(比例尺:5 μm);(e)基于溶剂蒸发和自发微乳液聚合生成的聚(乳酸-乙醇酸)共聚物(PLGA)核壳微粒;(f)具有甲基丙烯酸明胶(GelMa)内核和PLGA外壳的核壳微粒。
除了同时乳化多种内相流体的方法,还有其他制备具有各向异性特征的 Janus或多区软微粒的方法被开发出来。Min等报道了一种利用相分离产生多区微粒的策略,如图3(c)所示。由两种不混溶聚合物组成的均匀液滴由基于毛细管的微流控芯片制成。随着溶剂的蒸发,两种聚合物的相分离在固化过程中被触发。当溶剂彻底挥发,液滴完全固化得到橡子状Janus微粒。聚(N-异丙基丙烯酰胺)(PNIPAM)是一种广泛用于合成具有生物相容性软材料的聚合物。据研究,过饱和的N-异丙基丙烯酰胺(NIPAM)前体溶液会发生液-液相分离过程。Ghosh等制备了雪人形Janus水凝胶微粒,制备过程中只引入了一种单体水溶液形成液滴,液滴中水分挥发导致了NIPAM前体溶液的相分离并最终产生相应的Janus微滴[图3(d)]。随后通过紫外线(UV)照射使单体光交联,得到具有热响应性的异形PNIPAM微粒。
(三)核壳软微粒
核壳微粒是由壳层和封装在其内的不同形式的内核组成。得益于精巧的包裹结构,这些微粒展现了多样化的功能,如有效药物封装和可控递送。传统的大批量乳化途径所得的核壳软微粒在尺寸和构型上存在明显的不均匀性,这些微粒无法满足实际要求。液滴微流控能够制造尺寸和形状高度可控的均匀液滴,从而解决了这一难题。核壳微粒可以通过微流控技术结合相分离、自组装和表面反应等机制来获得。Yu等采用溶剂蒸发和自发微乳液聚合原理制备了新型核壳微粒,如图3(e)所示。Li等设计了包含甲基丙烯酸明胶(GelMa)内核和聚(乳酸-乙醇酸)共聚物(PLGA)外壳的单分散微粒。两种不同的生物聚合物溶液作为分散相和连续相,随后生成的双乳液液滴分别经过光聚合和溶剂蒸发后固化,如图3(f)所示。
(四)多孔软微粒
多孔微粒因其独特的形态和特性而在生物医学应用中具有重要意义。当使用液滴微流控平台生成多孔微粒时,表面及内部孔洞的形成机制可分为五种方法:触发聚合、牺牲模板、流体反应、自组装和流体光刻。反蛋白石结构是一种通过牺牲模板法制备的典型多孔构造。Chen等利用光子晶体正结构模板进一步获得了具有互连多孔结构的壳聚糖反蛋白石球。首先由二氧化硅纳米粒子以六方密堆积的形式自组装形成二氧化硅胶体晶体微粒(SCCB),随后将壳聚糖预凝胶溶液渗透到纳米粒子之间的缝隙中,并通过紫外照射进行聚合。在氢氟酸中去除SCCB模板后,形成了大孔凝胶支架[图4(a)]。壳聚糖反蛋白石微粒在促进细胞分布和迁移以及温度响应性药物释放方面表现出优异的性能。Hwangbo等通过溶剂蒸发诱导的相分离过程得到了具有凹坑形态和多孔内部的高尔夫球状微粒,其拥有比光滑球形微粒更大的比表面积。基于 Hwangbo等的成果,Lee等通过增加聚合物的比例进一步加大了表面凹陷程度,如图4(b)所示。除了应用单个液滴作为多孔微粒的模板外,具有多个内部液滴的双乳液体系也可以生成多孔微粒。Costantini等通过将液滴芯片与脉冲电场控制的二级分裂单元耦合,实现了可控多孔微粒的制造,如图4(c)所示。
图4. 多孔软微粒和其他类型复杂形状微粒的微流控制造。(a)SCCBs(i)、具有互连孔隙的反蛋白石微粒(ii)、一次灌胶SCCB微粒(iii)的表面及内部微观结构的扫描电子显微镜(SEM)图像,其中壳聚糖水凝胶填充孔隙(比例尺:500 nm);(b)高尔夫球状微粒的SEM图像;(c)在三种不同电压值下制备的乳液液滴及固化后多孔微粒的显微镜图像;(d)由变形液滴固化得到的片状和棒状聚(乙二醇二甲基丙烯酸酯)(EGDMA)微粒的图像(比例尺:200 µm);(e)通道中多相流及相应生成的纱线球状微粒的图像。
(五)具有复杂结构的多组分软微粒
具有其他复杂构型的多组分软微粒也表现出与众不同的特性。将可光固化液滴限制在具有各种尺寸和配置的微通道内,可以通过紫外线诱导的光聚合或者热聚合直接固化获得各向异性微粒。Xu等设计了一种综合体系,通过调整液滴尺寸和微流控通道的横截面形状来生产多种异形三丙二醇二丙烯酸酯(TPGDA)微粒。当液滴尺寸大于通道直径时,可将液滴重塑为非球形(如杆状、长方体和圆盘状)。Wang等在微通道内通过表面交联将均匀的微液滴封装到聚合物网络中,以产生含有液滴的纤维基质。通过拉伸和挤压纤维状基质,可以形成异形微滴,随后可生成多样化的微粒,包括片状、棒状和针状微粒。这些粒子能够在磁驱动下进行旋转和平移运动[图4(d)]。Miyama等应用微流控技术制备了具有特殊纱线球形状的凝胶微粒,如图4(e)所示。这些纱线球状微粒表现出了球体和纤维的双重优点,并且具有显著高于球形微粒的表面积与体积比(SA∶V)。
四、微流控纺丝技术制备多组分软纤维
微纤维包括具有各向异性特性的长丝和由这些长丝组成的材料。类似于天然纤维的结构和功能,人造软纤维的形状或长丝单元的排列对特定方向的拉伸强度或刚度有着关键影响。这些纤维材料在传感器、可穿戴设备等生物医学应用中发挥着重要作用。近来,微流控纺丝技术已被用于制造具有丰富形态和结构的纤维材料,其基本原理是中心射流在鞘流中的会聚和凝固。为了形成坚固的微纤维,无论通道几何形状如何,都必须减弱两相流体界面的不稳定性。固化中心流体的方法根据中心流体的性质大致可分为三种主要类型:光聚合、相转化和离子交联。
(一)微流控纺丝技术
微流控纺丝(microfluidic spinning)的机制源于微观通道内的液体层流。当多股流体相互接触时,它们之间的混合主要由界面扩散主导。前体溶液流可以通过快速固化原位转化为固体纤维,具体地,将含有前体溶液的样品泵入单独的入口通道,随后调整通道结构将纤维状流体变形为多种形态,最后引入适配的固化机制以生成固体纤维并保持理想形状。在此过程中,快速凝固至关重要。与传统的湿纺工艺相比,多样化的固化方法可以与微流控纺丝技术灵活结合,包括光聚合、化学/离子交联、相分离、溶剂蒸发/交换和界面组装等。这些固化策略使更广泛的材料用于纤维制造成为可能。许多软性生物材料已被用于制备纤维,包括藻酸盐、壳聚糖、GelMa、PLGA和聚乙二醇二丙烯酸酯(PEGDA)等。碳纳米管、金属纳米颗粒、氧化石墨烯(GO)和纤维素等添加剂也被引入纺丝过程中,赋予纤维特定的功能。此外,响应性聚合物组分(如NIPAM)可以赋予相应微纤维良好的动态响应性。目前已用于微流控纺丝的设备包括玻璃微量移液器、PDMS微通道、金属针管等。Meng等报道了应用微流控策略来设计坚韧且具有高黏弹性水凝胶微纤维的基本原理。制备过程结合了双网络的固化制造,包括琼脂相通过热转变的快速凝胶化以及随后紫外诱导的丙烯酰胺(AAm)基单体聚合。装置外部方形毛细管中的冰水有效地对内部毛细管进行冷却,从而生成前者的琼脂网络。
功能成分也可以在微纤维内同步原位合成,以赋予纤维理想的功能特性。微流控纺丝技术以连续流方式实现一步制造,因此适用于在微纤维中加入功能成分。通过调整微通道的尺寸和几何形状,可以制造出不同直径和结构的多种微纤维,包括空心、核壳、螺旋等复杂形状,其中部分产物是传统湿法或干法纺丝难以获得的。因此,微流控纺丝技术以其成本效益高、传质快、可控性高、可连续生产等优点,较好地适配了结构和功能可控微纤维的生产需求。
(二)核壳结构软性微纤维
核壳结构纤维可以使用同轴微流控芯片加以制造。Liu等开发了一种新型快速响应和高弹性水凝胶材料,随后将其泵入同轴微流控芯片,以生产具有核壳结构的热响应纤维,如图5(a)所示。由于其显著的温度响应性,纤维在温度升高的环境中会发生收缩。进一步地,整齐排列的纤维阵列的收缩会导致水凝胶变形,这一过程模拟了肌肉纤维的运动。
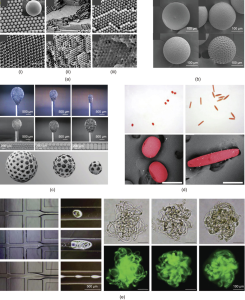
图5. 不同形状和结构的微流控软纤维。(a)具有温度响应性的核壳结构水凝胶微纤维(左侧图比例尺:1 mm;中间和右侧图比例尺:20 mm);(b)rGO/PU管状微纤维及其壁层FE-SEM图像;(c)螺旋形藻酸盐微纤维(比例尺:350 µm);(d)Janus、三重和异质软性微纤维的示意图和横截面荧光图像。
(三)管状软性微纤维
管状纤维可用于人体生理模拟、组织工程和药物输送等研究。管状(中空)纤维通常由具有三相同轴结构的微流控纺丝装置进行制备,其内、外径可以通过流速进行调节。Fujimoto等设计了一个十二微通道平行化微流控平台,以支持藻酸盐微管的高通量大规模生产。Daniele等通过原位光聚合的途径在方形微通道中制备了具有方形横截面的聚(乙二醇二甲基丙烯酸酯)(EGDMA)微管。Hu等通过应用包括明胶-羟基苯丙酸(Gtn-HPA)和聚砜在内的一系列材料制造管状微纤维,并将活细胞和生物活性成分[包括生长因子、细胞外基质(ECM)和营养物质]固定在水凝胶复合材料中。Huynh等设计了一种可拉伸的液体处理装置和一种由管状、导电微纤维制成的电化学阻抗免疫生物传感器[图5(b)]。其制备的管状微纤维由还原氧化石墨烯(rGO)、PU基质复合组成,构成了免疫生物传感器装置的微通道。管状微纤维的高导电性和可拉伸特性使其能够成为理想的检测人体汗液的电化学工作电极。
2023年苏州医疗器械展会Medtec China 16大特色展区,包括医用3D打印,骨科加工专区,及超精密激光加工、金属材料,部件和加工设备等研发设计领域,许多展商也将来到展会现场展示企业最新的产品及设计。
(四)螺旋软性微纤维
螺旋微纤维可以在特定的流体黏度和流速条件下在微流控装置中生成。通过整合多种流体,可以制备具有两个甚至多个分区的螺旋纤维材料。Yu等采用同轴毛细管连续微流控系统制备了螺旋微纤维,如图5(c)所示。当内相海藻酸钠流体被泵入CaCl2液流中时启动纺丝,随着Ca2+的扩散,快速凝胶化。有趣的是,当内、外相流速比增加时,内相流体的流动模式将从直线状态变为螺旋状态。由此可以精确调节螺旋状微纤维的直径和节距。
(五)Janus、三重和其他异质软性微纤维
目前,已有多项研究通过微流控纺丝技术制造了具有不同横截面形态的异质纤维,包括Janus、多组分和其他类型。为了生成Janus微纤维,通常会使用配备两个独立输入通道和一个外部输出通道的三相微流控装置。Jeong等使用有色和无色两种4-羟基丁基丙烯酸酯(4-HBA)溶液作为内相核心流制备了Janus水凝胶纤维。作为替代方案,Jung等应用具有简单二相设计的微流控装置来合成Janus的PU纤维。在其纺丝过程中,PU异氰酸酯基团与外相液流中的水发生反应并产生二氧化碳气泡,随后气泡向上迁移并形成多孔上界面,最终得到具有多孔和无孔双特性的Janus微纤维。除了Janus微纤维,Kang等还实现了不同颜色编码的三重藻酸盐微纤维的制备,他们采用的设备是由6个配备气动阀的进液管道构成,其纤维组成和形态可以获得全面精确调控。类似地,Bell等实现了三重“牙膏状”不对称超胶体微纤维的微流控纺丝制备。
Cheng等改进了一种简单的微纤维纺丝毛细管装置,该装置具有多个入口通道和分级射流通道,以获得结构更复杂的微纤维,如图5(d)所示。空心海藻酸盐微纤维是在先前的藻酸盐内相通道中再插入一个氯化钙(CaCl2)入口管来制造的[图5(d-i)]。一旦三种流体相互接触,溶液立刻在内外界面发生交联,随后可连续获得中空微纤维。类似地,通过在藻酸盐通道内嵌入几个CaCl2入口管来制造具有多个孔的微纤维,即增加毛细管装置中分层注入通道的数量来制备具有多个壳层的中空微纤维。使用多通道毛细管作为内相流道可实现多组分微纤维,如图5(d-ii)所示,在其中,海藻酸盐溶液的多种不同流体同时被泵入内相管并原位固化以形成多组分微纤维。在通道内,流体呈现层流状态,不同海藻酸盐溶液之间没有明显的扩散混合,因此微纤维不同组分之间的界面较为明显。如图5(d-iii)所示,通过结合中空纤维装置和多组分纤维装置的特征,还制备了具有多组分结构的中空微纤维。
(六)其他复合软性微纤维
除了上述常见结构的微纤维之外,大量研究聚焦在构建集成微粒的复合微纤维。Xie等使用一种新型的微流控纺丝方法展示了类似项链的结节纤维。他们还可控地制造了半球和花瓣结节纤维,如图6(a)所示。Shang等在一个包含同轴两相入口管的微流控芯片中集成了微流控纺丝和液滴乳化。通过合理控制流速,外层流体可以被夹断成纺锤状的液滴,这些快速凝胶化的液滴随后串在纤维上。所得微纤维具有周期性纺锤结,并产生接头,如图6(b)所示。Yu等则提出了一种内部包裹有液滴的纤维,其脱水后收缩成竹子状形态,如图6(c)所示。
图6. 其他复合软性微纤维。(a)具有半球形和花瓣形结的中空藻酸盐微纤维;(b)源自具有同轴两相入口管的微流控装置的纺锤结微纤维;(c)脱水后形成的仿生竹状微纤维;(d)收集在滚筒中的湿纺微纤维,以及通过钩针生成的3D支架来模拟肌腱和骨骼。
此外,已经开发了多种策略将微纤维组装成更高阶的结构,以创建各种 3D 宏观纤维来模拟组织。Calejo等通过组装具有特定形貌和成分的微纤维单元设计了一种3D纤维支架以模拟肌腱和骨骼,如图6(d)所示。为了实现这一目标,湿纺微纤维首先由聚己内酯(PCL)/明胶和PCL/明胶/羟基磷灰石(HAp)纳米颗粒生成。调整微流控中的不同流速以调整微纤维的直径和机械性能。然后,应用钩针技术构建3D纤维支架,并通过在其上培养干细胞来评估支架的生物学性能。除了编织之外,通过逐层堆叠微流控纺丝纤维实现了3D微结构,这种方法对于在生物学研究中构建组织模拟纤维网络具有重要意义。生物打印是一项很有前途的技术,可用于构建任意形状的3D纤维结构。通过将多个微流控通道与生物打印相结合,可以生成多组分微纤维组件。通常使用多入口Y形接头通道的微流控生物打印头,通过其进一步沉积材料和细胞。这些纤维材料在不同细胞的共培养、多重检测、生物传感等方面有着广泛的应用。值得一提的是,微纤维柔软的特性使其同时具备弹性,因此可以进一步组装成更复杂的织物,并产生特定的功能。
五、多组分软性生物材料的应用
微流控技术能够以均匀且高度可控的方式制造多种多组分软材料,通过特定成分的整合,赋予新材料一定的物理化学和生物学特性,如刺激响应能力、机械强度、生物相容性和柔韧性等。因此,微流控制备的多组分软性生物材料已被广泛应用于各个领域,尤其是生物医学领域。
(一)药物输送
活性剂的封装和控释对于药品食品、香料和化妆品的递送系统至关重要。为了确保有效的药物输送,通常将药剂以适当的剂量封装在某种载体中,并在特定的靶标位置释放。在药物输送应用中,宿主对工程软性生物材料的免疫反应是其功能化的重要因素。载药软性生物材料与细胞、组织和器官的相互作用有助于递送过程和随后的免疫反应。这些相互作用由颗粒的特性决定,包括化学组分、刚度、尺寸、形状、机械特性和表面电荷等。特别地,软性生物材料的表面形态往往在有效控制药物释放和局部免疫调节过程中发挥关键作用。然而,通过传统批量方法制备的药物载体存在包封率低和释放动力学控制不佳的问题,由微流控合成的材料能够一定程度上解决这些问题。Hussain等将界面不稳定性和微流控流动聚焦技术结合,生产出具有均匀尺寸和可控表面纹理的PLGA-b-PEG 微粒,如图7(a)所示,所得聚合物颗粒表现出不同的粗糙度,随后用于药物包封。有趣的是,通过改变微粒的表面凸起程度,可以调控载药效率和释放动力学。结果表明,这些尺寸约为3 μm的微流控聚合物颗粒可以触发细胞摄取行为并表现出优异的生物相容性。基于Hussain等的研究,Wang等借助溶剂挥发引起的界面不稳定性机制开发了具有可调粗糙度的各向异性花粉状褶皱微粒,如图7(b)所示。研究人员发现,这些具有高度表面纹理的药物载体可以很容易地黏附在结肠黏膜的前部。因此,药物可以装载到聚合物基质中,以进一步与人类结肠癌细胞和肠道炎症部位相互作用。
图7. 多组分软材料在药物输送中的应用。(a)用于药物封装的具有不同粗糙度的PLGA-b-PEG微粒;(b)易于黏附在结肠黏膜上并缓慢释放药物的高度褶皱微粒;(c)生物素化微凝胶,荧光图像显示了其捕获链霉亲和素的能力。
水凝胶微粒可用于移植细胞与免疫系统的物理隔离,例如,科学家进行了水凝胶包裹移植胰岛从而递送胰岛素以治疗糖尿病的研究。然而,克服移植后的过早免疫排斥反应一直是一项重大挑战。水凝胶微粒是胰岛移植的理想载体,它们可用于提供免疫保护屏障。与大片块状水凝胶相比,微粒的短扩散距离确保了营养物质和氧气与周围组织的有效交换,以维持胰岛存活并增强胰岛素从胰岛向周围脉管系统的转移。封装在微流控喷雾制备的海藻酸盐微粒中的胰岛可用作实现免疫隔离和增强治疗效果的平台,如图7(c)所示。有趣的是,一项研究通过比较宿主对直径100~1000 µm藻酸盐水凝胶微球的反应来验证材料尺寸的影响。调整微通道的几何形状或两相流体参数可以控制所得微球的大小,这有助于完善大小依赖性免疫反应的机制。
类似微粒,微纤维也可以作为药物载体。与微粒载体相比,纤维载体通常表现出较低的初始突释速率和受控的零级释放曲线,使其成为药物输送应用的理想材料。此外,圆柱形纤维通常具有较高的比表面积,且长度和横截面半径都可以轻易调节。这种可调节性对于实际应用中的药物输送系统至关重要。Marimuthu等成功地利用微流控制造了由两亲性三嵌段共聚物组成的微纤维支架,具有可控的孔隙率。他们将浸没沉淀和溶剂蒸发的效果与微流控纺丝工艺相结合来控制孔隙率。结果表明,纤维的孔隙率对模型纤连蛋白的释放具有显著影响。
医用金属以及医用橡塑材料的头部企业们悉数参加2023年苏州医疗器械展会Medtec China:韦恩堡、庄信万丰贵金属、田中贵金属(上海)、ELGILOY特种金属、三铃制线、江阴佩尔、麦迪斯、美国奥博锐、古河科技、沈阳中核舰航、路博润、NuSil、迈图、科思创、艾曼斯、塞拉尼斯、索尔维、龙海化工、江苏君华等。点击快速预登记。
(二)组织工程
组织工程已被证明有望用于组织/器官再生和移植。组织工程的原理涉及以下几个步骤:首先从患者的活检样本中分离出健康细胞,然后将细胞在体外扩增并接种或封装在载体中。工程组织构建体通常在体外预培养并转移到患者体内以替换受损组织,它们是由多种类型的细胞以及细胞外基质(ECM)组成的3D结构。某些组织的功能由多种信号介导,包括细胞间信号传导和细胞-细胞或细胞-ECM间相互作用。由微流控制备的微凝胶可以作为构建组织工程支架的基本单元。这些组织结构的应用已得到广泛研究,如骨/软骨再生、干细胞培养等。
结合微流控技术,可以根据需要生成具有层次结构的凝胶基质,以支持细胞培养并形成3D组件。细胞在其中会以类似于体内的形式进行组织,如纱线球形、核壳或管状结构。具有核壳结构的纤维可以用来包裹细胞,Onoe等通过应用毛细管微流控芯片制造了1 m长的核壳水凝胶微纤维,其中包裹ECM蛋白和分化细胞,囊括了肌肉细胞、内皮细胞和神经细胞。这些纤维可用于重建活体组织(如血管、肌肉纤维和神经束)的内在形态,模拟其功能特性,如图8(a)所示。
图8. 多组分软材料在组织工程和多重生物测定中的应用。(a)用于原代心肌细胞封装的蛋白微纤维;(b)扁平微槽藻酸盐纤维上的皮质神经元排列(比例尺:50 μm);(c)蝌蚪蛋形藻酸盐微纤维用于间充质干细胞(MSC)球体培养;(d)用于免疫测定和 HepG2 细胞培养的编码光子晶体(PhC)微球;(e)与目标miRNA孵育后,三种不同结构色编码微球的光学显微图像和荧光图像。
广泛的研究已经报道了使用微流控纺丝微纤维来诱导不同的细胞取向生长,如成肌细胞、成纤维细胞和心肌细胞等。Kang等设计了一种表面刻有微型凹槽(直径小于100 μm)的藻酸盐纤维,随后将神经元细胞接种到带凹槽的纤维上[图8(b)],细胞随着凹槽排列生长。此外,通过其他方法制造的图案化微纤维也证明了其对细胞引导的能力。Yang等构建了具有定向亚微米形貌的藻酸盐纤维,可以通过调控微流控纺丝技术的参数来调节其结构。培养在图案化纤维表面的细胞展示出沿纤维轴有序扩散的趋势。Nguyen等通过应用三相流PDMS微流控装置,得到了蝌蚪蛋形的复合软性微纤维,如图8(c)所示。随后,这些微纤维为细胞培养创建了3D微孔模板,从而增强了软骨细胞的分化能力以用于骨修复。
(三)多重生物检测
在药物研发和临床诊断中,迫切需要高效的多重检测策略。一种有潜力和前景的检测载体是使用编码微球,对有关其特定成分的信息进行编码,以实现简单的识别。微流控技术是均一合成软性编码微载体的有效途径。所得微粒具有高灵活性、快速反应时间、较少试剂消耗和良好重复性的特性。与包裹染料色素或荧光分子进行编码的各向同性微载体相比,各向异性多组分软微粒可以有效地实现编码量的放大。除了微粒本身携带的编码信息,其自身形状、组成和某些图案化的表面特征等也可以成为附加的多种编码元素。因此,各向异性多组分编码微粒的检测效率与传统的各向同性编码载体相比有所提高。利用微流控多重乳液液滴模板,可以制备出大量精美的多组分编码微粒。Kim等利用次序乳化微流控方法通过水包油包水(W/O/W)液滴将水溶性红色、绿色和蓝色(RGB)着色颜料封装在透明的乙氧基化三羟甲基丙烷三丙烯酸酯(ETPTA)树脂中,得到了多组分编码微胶囊。该系统结合了光学和图案编码方法,通过调节流速实现对胶囊尺寸和成分的精确控制。经过表面修饰后,这些微胶囊可用于抗原抗体的特异性识别和检测。Shang等通过液滴微流控生成具有半透膜壳和纳米粒子组装内核的微胶囊,得到了一种光子晶体(PhC)气泡编码微载体[图8(d)],其中,包封的胶体纳米颗粒通过溶剂挥发在微囊内壁自组装形成中空球形光子晶体。通过调整微泡的总密度以匹配检测溶液的密度,从而使它们保持悬浮状态。这种策略提高了编码的移动性,从而提高了检测效率。Bian等用GO修饰PhC编码微球以量化测定肿瘤相关的 microRNA。GO被封装在编码载体表面,能够增强载体的稳定性和对非相干光散射的抵抗力,使其具有恒定的特征反射峰。此外,固定在编码载体外的GO可以与miRNA探针结合,实现有效筛选,如图8(e)所示。
六、总结与展望
软性生物材料长期以来一直被应用于组织工程、再生医学、软体机器人、可穿戴设备和生物诊断等生物医学领域。近年来,为了整合多种功能,这些材料的结构和成分呈现多样化的趋势。随着制造技术的进步,尤其是微流控技术的发展,这一理念已成为现实。本文总结了多组分软性生物材料的微流控制备。我们首先简要介绍了典型的软性聚合物,主要包括水凝胶和弹性体,以及它们的常见交联方式。接着,我们描述了如何通过微流控方法将这些聚合物塑造成具有可微调配置的多组分软性生物材料,主要产物形式为多组分颗粒和微纤维。进一步地,我们详细讨论了这些多组分软性生物材料在生物医学领域的应用。
尽管近几十年来取得了令人振奋的成就,但多组分软性生物材料的微流控合成及其在生物医学领域的应用仍面临挑战。首先,开发新的软性材料来源。以水凝胶为例,为了实现特定的功能,改变化学成分或合成因子可能会产生具有所需功能和应用价值的新型生物材料。为实现这一目标,深入了解软性生物材料的化学、机械和流变行为是先决条件。应持续努力研究多种材料体系,包括基本聚合物及其复合材料。其次,为了应用微流控技术更好地制造多组分软性生物材料,需要更复杂的通道设计来容纳新的组件。例如,微流控中使用的一些聚合物溶液或熔体是非牛顿液体,应考虑它们在微尺度上的流体行为。另外,还需要提高通量。由于微通道的尺寸限制,目前微流控量产受到了极大的影响。要实现工业级的批量大规模生产,需要采用新颖稳定的可扩展芯片设计。目前的成果表明,高度单分散的液滴和相应固化微粒可以通过平行化获取。然而,关于微纤维和其他复杂复合材料的平行合成研究少有报道。最后,多组分软性生物材料的利用仍处于起步阶段,尤其是在临床转化的实际应用方面。对于可预测的生物医学应用,迫切需要对多组分软性生物材料在体内的功能和安全性进行更全面深入的研究。
为了突破以上问题,未来的研究可能集中在两个主要方向:探求新型材料成分以及开发新型微流控平台,以支持软性生物材料的制备并实现大规模生产。可结合集成电路利用系统微流控工艺实现高质量复合材料的规模化生产。此外,将软性生物材料材料与包括3D生物打印在内的其他生物制造技术进一步融合,能够促进仿生实验室培养组织的制造。可以预见,基于在软物质、物理、化学、生命科学、材料科学以及技术创新方面的多学科交叉研究,有望解决当前微流控及软性生物材料方面的限制。我们相信,结合微流控技术的多组分软性生物材料将为生物医学领域提供新思路并带来巨大进步。
文章来源:











