2024上海医疗器械创新展Medtec新技术-血管内影像创新发展-光学相干断层扫描(OCT)
2024-07-10
前期阶段
该概念最早于1991年由麻省理工学院(MIT)的James Fujimoto、Eric Swanson和David Huang提出,同时在日本由Naohiro Tanno也提出这一概念。James Fujimoto专注于光学,为了满足“更好地观察人体内部结构”的临床需求,受到研究中高速摄影和激光的启发,探索使用光学代理超声技术的研究;Eric A. Swanson 专注激光通信和光纤网络技术研究,提出了使用干涉仪测量光波反射时间和距离,激发了James Fujimoto的灵感,觉得这一方法具有极高的分辨率,便邀请Eric A. Swanson加入他的团队;David Huang 是 James Fujimoto 实验室的博士后。三人合作于1991 年,发表了第一篇描述 OCT 技术原理和应用的论文。最初,是通过分析反射的近红外光来增强各种身体组织的横截面成像,特别是为了进一步表征人眼的视网膜和视盘。鉴于其高分辨率和精细区分组织平面的能力,进一步将这一概念应用于冠状动脉血管,期待在动脉壁复杂病变中探索影像活检。
那么如何进行成像?2024上海医疗器械创新展Medtec表示其通过对样本的纵向和横向扫描,生成了来自样本和参考镜的光反射,并进行比较并最终数字化,生成图像。通过这种方式,Fujimoto在解剖的冠状动脉标本中生成了一些最早的脂肪、钙化和纤维斑块的光学图像。取得这一初步成功后,Fujimoto与Carmen Puliafito和Eric Swanson于1992年创立了第一家商业OCT公司——Advanced Ophthalmic Devices,这为未来他们技术的冠状动脉内应用奠定了基础。
OCT原型和系统
1995年,通过麻省总医院的Brezinski等人与麻省理工学院的Fujimoto和Tearney的合作,开发了第一个OCT导管原型。他们的1.1毫米导管内窥镜由单模光纤组成,贯穿整个设备,在远端安装了一个微棱镜和镜子。与机械旋转的IVUS设备一样,这个导管也旋转以环绕血管周围进行扫描,并可通过沿着血管的回拉来获得图像,速度可达30帧/秒。
1996年,Fujimoto和Brezinski在解剖的人体腹主动脉段上测试了他们的原型,首次使用他们的导管系统识别了动脉粥样硬化、钙化和薄壁脂质斑块。Fujimoto的其中一张早期专利图示显示了这一点。
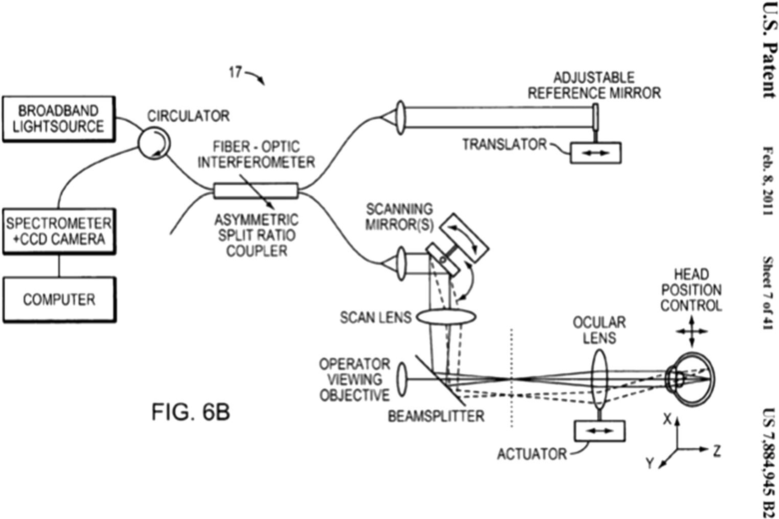
Fujimoto 2011美国专利的示意图
然而,他们的观察主要是在血管壁中没有血液的“空气中”环境下进行的,血管壁中没有血液,这对初始评估模型来说是具有局限性(验证与尽量模拟人体环境和疾病状态)。2002年,Tearney使用一个非商业化的1.06毫米(3.2 Fr)改进型IVUS导管,首次在活体患者中展示了冠状动脉内OCT的结果。他们将OCT图像与同一动脉生成的IVUS系统图像进行了比较,并同样评论了OCT图像显著更高的分辨率,能够识别出如内膜增生、内弹力层和外弹力层之间的边界、薄纤维帽和其他IVUS无法检测到的解剖。
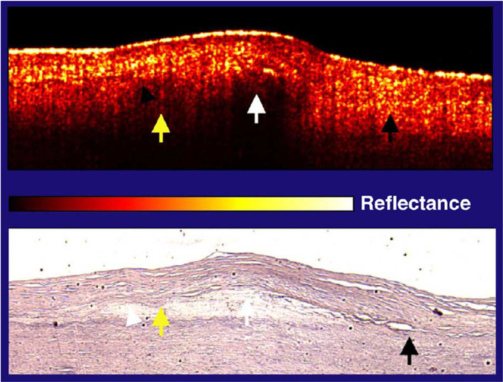
1996年初OCT薄纤维帽脂质斑块界面图像
LightLab Imaging开发了第一个临床可用的OCT成像系统(M2/M3 OCT系统)及其相关的成像导管(ImageWire)。

LightLab公司生产的早期OCT成像导管
2024上海医疗器械创新展Medtec同期推出ADTE 高端有源医疗装备技术展汇集国内外高端医疗器械生产厂商,助力中国高端医疗器械国产化。此外,现场还将举办有源医疗设备核心部件与技术论坛,议题涵盖物联大趋势下传感器如何助力前端数据采集、探测器在有源设备中的应用及发展、特殊材料在有源部件上的使用等。现在注册参观即可免费参会>>>
第一个成像导管使用0.41毫米光纤线结合导丝球囊封堵和生理盐水冲洗系统,以提供“无血”视野,以确保图像质量。自动回调控制台从目标系统检索光纤线以生成图像 一个自动回拉控制台从目标位置探测回收光纤线以生成图像。这个系统的OCT分析基于时域模态,其中通过物理地改变到参考镜的距离来确定组织深度,从而限制了图像生成的速度。
早期OCT系统的局限性
早期OCT系统,特别是M2/M3系统的主要局限性是在血管成像时需要一个“无血”视野。近场中的红细胞引起显著的光散射,导致图像质量不佳。早期使用是将一个球囊低压扩张放置在病变的近端,以减少流向感兴趣区域的血流达30秒。另一种技术利用每秒8-10毫升的生理盐水反复注射,有时可以清除一个区域长达2秒。这些技术不仅有导致暂时性缺血和球囊扩张部位血意外损伤管的风险;而且操作过程本身也很费力,对严重狭窄具有挑战性。球囊阻塞会阻止评估口部病变或左前降支或左回旋支动脉的近端病变,并且不推荐封堵了未受保护的左主干。
另一局限是相对较低的4-15帧/秒的帧速率和0.5-3毫米/秒的回拉速度。低帧速率还有可能产生运动伪影。最后,OCT在血管表面附近提供了无可挑剔的分辨率,但光的穿透深度有限,无法进一步评估深层斑块特征,如总脂质负担或血管重构的变化。
从新一代OCT到现代系统
1990年代后期和2000年代初期开发的新一代OCT系统解决了第一代系统的许多结构和技术限制。LightLab推出了频域OCT系统(C7-XR与Dragonfly成像导管),以应对M2/M3系统更繁琐的时间域模式。频域系统使用一个固定的镜子和一个可变波长光源,根据时间和波长测量数据。这显著提高了图像检索的便利性,使OCT速度快了近十倍。现在可以在不到3秒内成功成像一个50毫米的血管节段。这些新系统还配备了每秒高达4毫升的生理盐水注射系统,几乎完全消除了对持续低压球囊阻塞的需求。更粘稠的碘对比剂成为清除血液的优选介质。Tearney等人在冠状动脉系统中首次测试了频域系统,他们的结果表明,所有以前的冠状动脉内OCT成像优势在这个更快、更高效的系统中依然存在。
OCT在国内外
目前,OCT系统广泛应用于冠心病精准诊疗中。在美国有两家主要公司获得批准使用。LightLab,第一套系统的官方开发者, 2010年LightLab被St. Jude Medical(圣犹达)收购,2016年圣犹达被Abbott(雅培)收购,继续生产C7XR系统以及Ilumien Optis系统。后者系统现在能够简化OCT图像处理,实时帮助指导支架直径和长度选择。Conavi Medical在2018年获得FDA批准,其Novasight Hybrid系统结合了IVUS和OCT为一个导管系统。Terumo Corporation(东京,日本)也开发了OCT系统。OCT技术的发展:多模态融合;AI应用可以自动检测支架及其在血管内位置;增强对比和分子OCT是一个专门使用微球体、纳米粒子和其他染料的子领域,旨在增强组织内光的传输;AI协助的实时自动组织判别分类和计算也是研发的热点。
OCT在中国深圳微光医疗、南京沃福曼医疗、天津恒宇医疗、苏州阿格斯(微创)……(之后根据时间给大家分享各个产品特点)
电视剧问心中使用OCT检查
致敬
OCT技术是一种新的高分辨率成像技术,这种新的成像技术通过利用光束来观察人体组织内的微观结构,能够实时获得高分辨率横截面图像,而无需身体接触。2023年三位OCT发明者James G. Fujimoto、David Huang和Eric A. Swanson获拉斯克奖。

2024上海医疗器械创新展Medtec创新感悟
1、创新需要团队,未来的创新发明需要不同专业、不同来源和不同机构的人相互协作。一起来实践葛校长提出的“以临床为导向的有组织创新”,在创新的每个环节赋能加速,促进中国原创发展。
2、创新需要耐力,一个创新产品的孵化到发展再到成熟,是一个不断迭代、打磨和优化的过程,面对失败,总结经验是提示我们继续的方向,面对成功,是鼓励我们继续前行,在繁华中思考,在寂寞中蜕变,在跌宕起伏中螺旋成长。
3、创新需要静心的思考:OCT实际上是超声波或雷达的光学模拟,结合光的波长短的特点,以获得更高的微观分辨率。
4、创新需要注意每一个细节:OCT体外验证血管没有血液,如何破除红细胞对成像的影响?如何提高成像速度?
5、创新不是卷卷卷,而是协同一个更广泛的创新生态:OCT的发现这项技术不是超声波、CT或MRI的替代品,而是一种具有独特优势和互补优势的不同工具。核磁共振、CT和超声波可以穿透身体深处,形成全身图像,但分辨率有限。OCT可以进行“光学活检”,以显微分辨率成像地下结构,而无需切除和处理标本。每个创新者可以关注疾病诊治的不同阶段,一种创新产品的不同阶段,创新产品诊治生态的不同补充和优化,这样可以避免资源合理高效优化分配。
文章来源:











