质量管理
-
2022.02.10
质量体系丨植入医疗器械生产,参考这些规章要求
为帮助企业建立合规的植入性医疗器械生产质量管理体系,本文列举了其中重点环节的审查要求,供大家参考及自查对于自行具备产品灭菌能力的植入性医疗器械生产企业,其出厂检验项目规定对产品进行无菌检验,可按照规定执行……
阅读更多 -
2022.01.27
设计开发输入与医疗器械注册申报资料关系探讨
医疗器械的设计开发是决定产品质量的重要过程,而设计开发输入又是整个设计开发过程的关键环节,为后续的设计开发验证和确认奠定了基础,从而对注册申报资料产生重要影响……
阅读更多 -
2022.01.21
UDI如何实施?如何编制?全在这儿了!
在12月29日发布的《关于在eRPS系统提交医疗器械唯一标识有关事项的通告》中提到:对于列入《第一批实施医疗器械唯一标识的产品目录》中的医疗器械……

阅读更多 -
2022.01.17
如何确保医疗器械的安全有效?
当医疗器械的安全性可基于确凿的科学证据来确定,该科学证据表明:在预期用途和使用条件下,且具备充分的指导和对不安全使用的警示的情况下,使用该器械对健康带来的可能益处超过可能风险……
阅读更多 -
2022.01.11
无菌医疗器械包装设计和开发如何评价?
无菌医疗器械包装设计和开发是一项复杂而重要的系统性工作,无菌医疗器械包装材料的选择是重中之重。无菌医疗器械包装材料的选择应结合预期内包装物实际情况进行全面的评价,一般考虑如下要求……
阅读更多 -
2022.01.06
独家|如何让你的全球性医疗器械翻译内容更加本地化?
通过多语言医疗器械标识的严苛标准会很难。实现这一目标需要准确的翻译、本地化、测试和验证。当然,关键是提前计划和充分准备……
阅读更多 -
2022.01.05
无菌医疗器械生产质量管理规范检查要点指南
本指南可作为北京市药品监督管理局组织、实施的医疗器械注册质量管理体系现场核查、《医疗器械生产许可证》现场核查、医疗器械生产监督检查等各项检查的参考资料……
阅读更多 -
2021.12.09
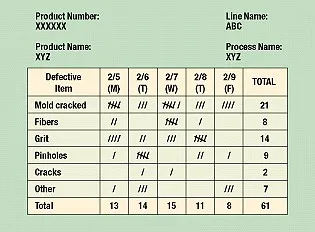
七个改进质量的基本工具
只有了解解决问题或质量改进的基本过程,才能运用质量工具更快更系统地开展工作,下面介绍了七个改进质量的基本工具……
阅读更多 -
2021.12.03
医疗器械注册是否必须取得ISO13485认证证书?
首先说一下答案,答案是不需要。申请医疗器械注册证不是必须提供ISO13485认证证书。只是你们公司拿注册证是必须通过药监局的体系考核的(专业名词是GMP体系),该体系考核和ISO13485差不了多少……

阅读更多 -
2021.11.23
医疗器械注册体系审核是如何进行体系核查的
经历过体系考核的人都知道,一般来体考的审核员至少有2名,其中1名组长,1名组员,审核时间至少为1天时间,审核员要在1天之内对企业进行全面的核查,并作出是否合规的评价,必须抓审核重点,本文总结了一些审核要点,仅供参考……
阅读更多











